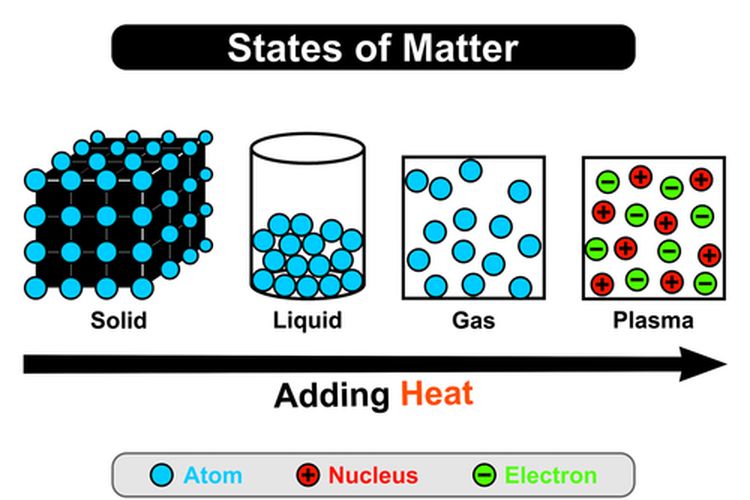
Teori Kinetik Gas dan Hukumnya
P1V1 = P2V2
Keterangan
P1 = tekanan gas pada keadaan 1 (n/m kuadrat)
V1 = volume gas pada keadaan 1 (m kubik)
P2 = tekanan gas pada keadaan 2 (n/m kuadrat)
V2 = volume gas pada keadaan 2 (m kubik)
Pada suhu konstan, jika tekanan atau volume gas berubah, maka variabel yang lain juga berubah.
Proses isometis adalah pada saat volume bertambah, maka tekanan gas akan berkurang.
Baca juga: Macam-Macam Sendi dalam Tubuh
Hukum Charles
Selain ditentukan oleh tekanan, volume gas dalam ruang tertutup juga dipengaruhi oleh suhu.
Jika suhu gas dinaikkan, maka gerak partikel gas akan semakin cepat sehingga volumenya bertambah.
Bila tekanan tidak terlalu tinggi dan dijaga konstan, volume gas akan bertambah terhadap kenaikan suhu.
Hukum Charles berbunyi demikian:
"Apabila tekanan gas yang berada dalam ruang tertutup dijaga konstan, maka volume gas berbanding lurus dengan suhu mutlaknya".
Dapat dirumuskan sebagai berikut:
V/T = Konstan atau V1/T1 = V2/T2
Keterangan:
V1 = volume gas pada keadaan 1 (meter kubik)
T1 = suhu mutlak gas pada keadaan 1 (K)
V2 = volume gas pada keadaan 2 (meter kubik)
T2 = suhu mutlak gas pada keadaan 2 (K)
Hukum Gay Lussac
Apabila botol dalam keadaan tertutup dimasukkan ke api, maka botol tersebut akan meledak.