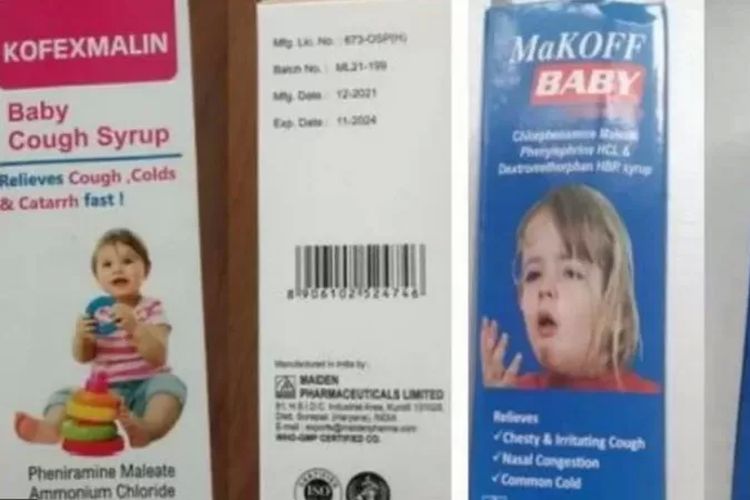
JAKARTA, KOMPAS.com - Badan Pengawas Obat dan Makanan (BPOM) Indonesia memastikan empat sirup obat batuk asal India tidak terdaftar di Indonesia.
Keempat sirup ini dituduh menjadi penyebab gagal ginjal pada anak di Gambia karena mengandung etilen glikol.
Keempat sirup tersebut adalah Promethazine Oral Solution, obat batuk sirup bayi Kofexmalin, obat batuk sirup Makoff, dan obat demam sirup Magrip N.
Baca juga: Perusahaan India Setop Produksi Sirup Obat Batuk Setelah Kematian Puluhan Anak di Gambia
Keempatnya diproduksi oleh Maiden Pharmaceuticals Limited, India.
1. India sudah perintahkan penghentian produksi
Pihak berwenang India sudah memerintahkan Maiden Pharmaceuticals Limited untuk menghentikan sementara produksi obat batuk yang diduga memicu kematian puluhan anak di Gambia.
Menteri Kesehatan Negara Bagian Haryana, Anil Vij mengatakan hasil inspeksi di pabrik Maiden Pharmaceuticals menunjukkan sejumlah pelanggaran terhadap praktik yang baik.
Organisasi Kesehatan Dunia (WHO) telah merilis peringatan kepada seluruh dunia atas bahaya yang bisa ditimbulkan empat obat batuk sirup yang diproduksi Maiden.
Obat-obat itu, menurut WHO, boleh jadi terkait dengan penyakit gangguan ginjal akut dan kematian puluhan anak pada bulan Juli, Agustus, dan September.
Baca juga: Obat dari India Diduga Sebabkan Gagal Ginjal Akut di Gambia, Apakah Beredar di Indonesia?
2. Yang terjadi di Gambia
Pekan lalu, Organisasi Kesehatan Dunia (WHO) mengeluarkan peringatan terhadap empat merek sirup obat batuk yang disebut menyebabkan kerusakan ginjal akut, menyusul laporan dari Gambia tentang sejumlah anak yang didiagnosis dengan masalah ginjal serius.
Menurut WHO, analisis laboratorium dari obat batuk sirup ini mengonfirmasi bahwa obat itu memiliki kandungan dietilen glikol yang berlebihan dan etilen glikol sebagai kontaminan.
Pihak berwenang India dan produsen sirup obat batuk, Maiden Pharmaceuticals, mengatakan sirup ini hanya diekspor ke Gambia.
We're not selling anything in domestic market. We've been obtaining raw materials from certified & reputed companies. CDSCO officials have taken samples & we are awaiting the results: Maiden Pharmaceuticals Ltd on deaths of 66 children in Gambia allegedly due to their cough syrup pic.twitter.com/HFEJbx1POx
— ANI (@ANI) October 8, 2022
3. Respons Indonesia
Dalam siaran pers pada Senin (17/10/2022), Badan Pengawas Obat dan Makanan (BPOM) menyatakan keempat produk yang ditarik di Gambia tersebut tidak terdaftar di Indonesia dan hingga saat ini produk dari produsen Maiden Pharmaceutical Ltd, India tidak ada yang terdaftar di BPOM.
BPOM menyatakan bahwa telah menetapkan persyaratan pada saat registrasi bahwa semua produk obat sirup untuk anak maupun dewasa, tidak diperbolehkan menggunakan dietilen glikol (DEG) dan etilen glikol (EG).
"Namun sebagai langkah kehati-hatian, BPOM juga sedang menelusuri kemungkinan kandungan DEG dan EG sebagai cemaran pada bahan lain yang digunakan sebagai zat pelarut tambahan," sebut BPOM.
Baca juga: Sirup Obat Batuk Buatan India Diduga Picu Kematian 66 Anak di Gambia
Lebih lanjut, BPOM akan melakukan langkah-langkah pengawasan intensif terhadap obat-obat terkait dan akan segera menyampaikan hasilnya kepada masyarakat.
BPOM pun mengimbau masyarakat agar membeli obat yang sudah mendapat izin edar dari BPOM.
"Masyarakat agar lebih waspada, menggunakan produk obat yang terdaftar di BPOM yang diperoleh dari sumber resmi, dan selalu ingat Cek KLIK (Cek Kemasan, Label, Izin Edar, dan Kedaluwarsa) sebelum mengonsumsi obat," ungkap BPOM.
Belum diketahui apakah dietilen glikol (DEG) dan etilen glikol (EG) merupakan penyebab kasus gangguan ginjal akut di Indonesia.
Kasus gangguan ginjal akut di Indonesia dilaporkan telah menyerang lebih dari 150 anak, sementara Kementerian Kesehatan RI telah menerbitkan panduan untuk menangani penyakit tersebut.
Ikatan Dokter Anak Indonesia, IDAI sampai Jumat (14/10/2022) mencatat 152 anak terkena gangguan ginjal akut (AKI) dengan mayoritas berusia 1-5 tahun.
Baca juga: 66 Anak-anak Meninggal di Gambia Diduga Terkait Penggunaan Obat Batuk Buatan India
4. Tentang produsen obat asal India, Maiden Pharmaceuticals
Maiden Pharmaceuticals mengeklaim pihaknya mematuhi standar kontrol kualitas yang diakui secara internasional.
Meski begitu, beberapa produknya gagal memenuhi standar kontrol kualitas tingkat nasional atau negara bagian di India.
Catatan resmi di India menunjukkan…
-
![]()
Perusahaan India Setop Produksi Sirup Obat Batuk Setelah Kematian Puluhan Anak di Gambia
-
![]()
Obat dari India Diduga Sebabkan Gagal Ginjal Akut di Gambia, Apakah Beredar di Indonesia?
-
![]()
India Hadapi Pandemi "Kuman Super" yang Kebal Antibiotik
-
![]()
Catat Sejarah, India Sukses Tembakkan Rudal Balistik dari Kapal Selam Nuklir Buatan Lokal
-
![]()
Bagheera, Macan Tutul Hitam Langka yang Dinamai Seperti karakter Jungle Book Terlihat di India
-
![]()
Sirup Obat Batuk Buatan India Diduga Picu Kematian 66 Anak di Gambia
-
![]()
66 Anak-anak Meninggal di Gambia Diduga Terkait Penggunaan Obat Batuk Buatan India
-
![]()
Bus Berisi Tamu Pernikahan Jatuh ke Jurang di India, 25 Tewas
-
![]()
Salju Himalaya India Longsor, 4 Orang Tewas, Puluhan Masih Hilang
-
![]()
Jet Tempur India Kawal Pesawat Iran karena Ada Ancaman Bom, Ternyata Palsu















































![[POPULER GLOBAL] Rudal Tua Tapi Canggih | Miss Buenos Aires Usianya 60](https://asset.kompas.com/crops/YTjScCsHqpmAVbtM641X0s2pObo=/0x0:1998x1332/177x117/data/photo/2024/01/06/6598c62481cfd.jpg)






















