Macam-Macam Model Atom: Dalton, Thomson, Rutherford, dan Bohr
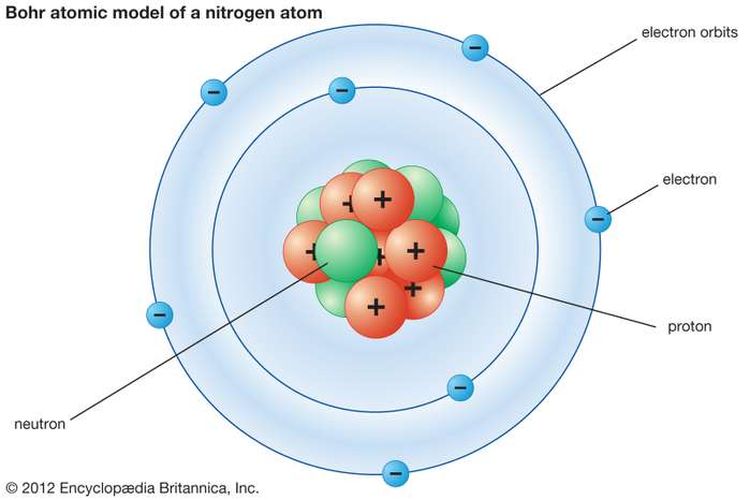
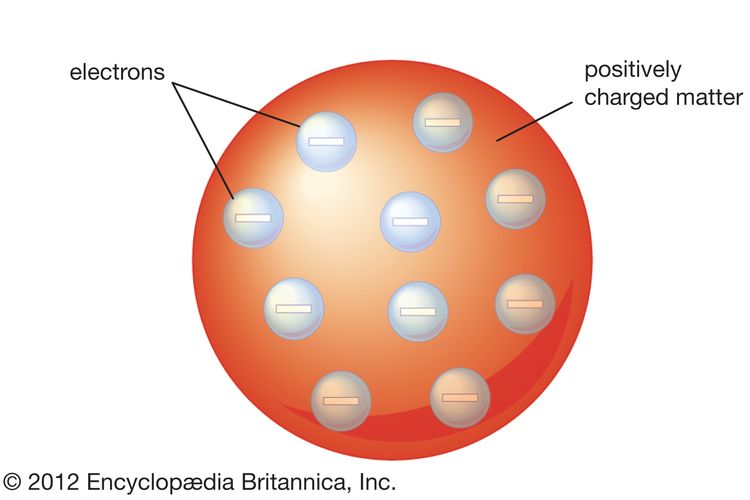
Atom adalah bola berongga yang tersusun dari inti atom dan elektron yang mengelilinginya.
Inti atom bermuatan positif. Selain itu, massa atom terpusat apda inti atom.
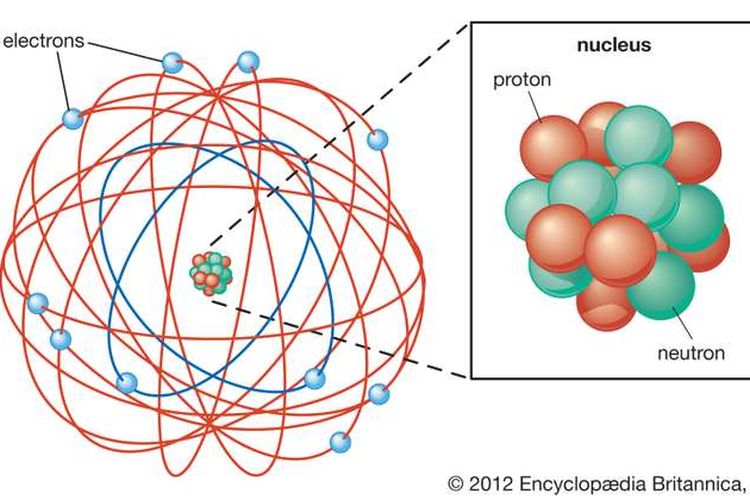
Model ini persis seperti bagaimana planet mengelilingi matahari.
Namun model atom Rutherford tidak dapat menjelaskan mengapa elektron tidak jatuh ke dalam inti atom.
Berdasarkan teori fisika, gerakan elektron mengitari inti ini disertai pemancaran energi.
Ini menyebabkan lama-kelamaan energi elektron akan berkurang dan lintasannya makin lama akan mendekati inti dan jatuh ke dalam inti.
Meski demikian, Rutherford telah berjasa mengenalkan konsep lintasan atau kedudukan elektron yang kelak disebut dengan kulit atom.
Baca juga: Kelebihan dan Kekurangan Teori Atom Rutherford
Model Atom Bohr
Niels Bohr, ahli fisika dari Denmark adalah ilmuwan pertama yang mengembangkan teori struktur atom pada 1913.
Teori tentang sifat atom yang didapat dari pengamatan Bohr:
- Atom terdiri dari inti yang bermuatan positif dan dikelilingi oleh elektron yang bermuatan negatif di dalam suatu lintasan.
- Elektron bisa berpindah dari satu lintasan ke lintasan yang lain dengan menyerap atau memancarkan energi sehingge energi elektron atom itu tidak akan berkurang
- Jika berpindah ke lintasan yang lebih tinggi, elektron akan menyerap energi. Jika berpindah ke lintasan yang lebih rendah, elektron akan memancarkan energi.
- Kedudukan elektron-elektron pada tingkat-tingkat energi tertentu-tertentu yang disebut kulit-kulit elektron.
Model atom Bohr menunjukkan bahwa atom terdiri dari beberapa kulit. Kulit ini adalah tempat berpindahnya elektron.
Namun model atom Bohr memiliki radius dan orbit. Ini tidak sesuai dengan Prinsip Ketidakpastian Heisenberg yang menyatakan radius tidak bisa ada bersamaan dengan orbit.
Selain itu, model atom Bohr juga tidak menjelaskan Efek Zeeman. Efek Zeeman adalah ketika garis spektrum terbagi karena adanya medan magnet.
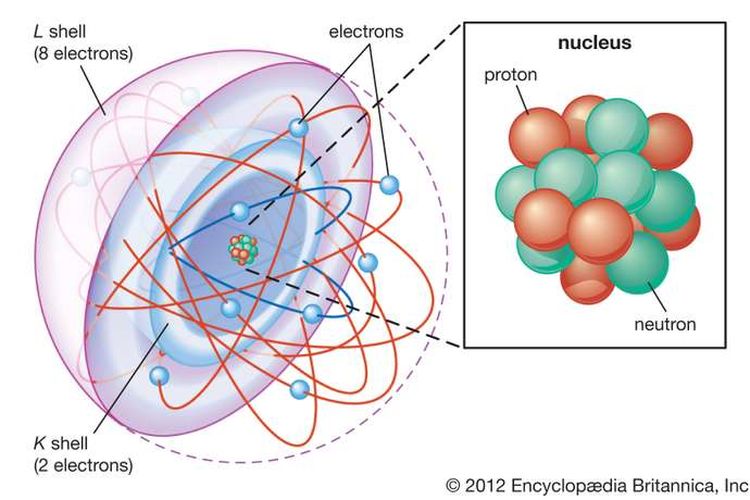 Model atom modern
Model atom modernModel atom modern
Setelah abad ke-20, pemahaman mengenai atom makin terang benderang.
Model atom modern yang kita yakini sekarang adalah penyempurnaan oleh Erwin Schrodinger pada 1926.
Schrodinger menjelaskan partikel tak hanya gelombang, melainkan gelombang probabilitas.