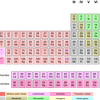
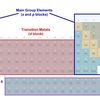
Mengapa Senyawa Unsur Transisi Berwarna?

KOMPAS.com – Senyawa unsur transisi umumnya berwarna. Hal ini disebabkan karena …
- Orbital d-nya terisi penuh
- Orbital d-nya tidak terisi
- Pengisian terakhir pada orbital d
- Bersifat paramagnetik
- Elektron dalam keadaan berpasangan
Jawabannya adalag c. pengisian terakhir pada orbital d. Untuk lebih memahaminya, berikut penjelasan mengapa senyawa unsur transisi berwarna!
Baca juga: Sifat-sifat Unsur Golongan Logam Transisi Periode 4
Tidak seperti senyawa dari logam non transisi yang tidak berwarna, senyawa unsur transisi memiliki berbagai macam warna.
Dilansir dari Angelo State University, unsur transisi memiliki orbital d yang tidak terisi penuh dengan elektron.
Pengisian terakhir pada orbital d inilah yang menyebabkan senyawa unsur transisi berwarna.
Dilansir dari Chemistry LibreTexts, ketika ligam menempel pada logam transisi untuk membentuk senyawa kompleks, maka elektron pada orbital d terpecah menjadi orbital berenergi tinggi dan orbital berenergi rendah.
Baca juga: Dampak Penggunaan Unsur Golongan Logam Transisi Periode 4
Elektron yang berada pada orbital berenergi rendah dapat berpindah ke orbital d berenergi tinggi dengan dorongan foton.
Di mana energi foton dari cahaya diserap untuk mendorong elektron dari orbital rendah ke orbital tinggi.
Adapun, kesenjangan energi pada orbital d senyawa unsur transisi berkaitan dengan foton panjang gelombang tertentu.
Misalnya, elektron memerlukan panjang gelombang yang menyebabkan warna kuning untuk berpindah.
Baca juga: Apa itu Panjang Gelombang?
Dilansir dari Chemguide, cahaya kuning akan diserap dan karena energinya digunakan untuk mendorong elektron, maka akan meninggalkan warna lain.
Yaitu, warna biru karena warna biru adalah warna komplementer dari kuning. Maka, senyawa transisi tersebut akan memiliki warna biru.
Simak breaking news dan berita pilihan kami langsung di ponselmu. Pilih saluran andalanmu akses berita Kompas.com WhatsApp Channel : https://www.whatsapp.com/channel/0029VaFPbedBPzjZrk13HO3D. Pastikan kamu sudah install aplikasi WhatsApp ya.