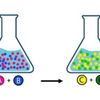
Faktor yang Memengaruhi Pergeseran Kesetimbangan

KOMPAS.com – Setiap reaksi kimia memiliki kesetimbangannya sendiri. Kesetimbangan dapat dipengaruhi oleh berbagai faktor. Di bawah ini faktor yang tidak memengaruhi pergeseran kesetimbangan adalah:
- Konsentrasi
- Katalis
- Suhu
- Tekanan
- Volume
Jawabannya adalah b. Katalis. Untuk mengetahui alasannya, berikut adalah faktor-faktor yang memengaruhi pergeseran kesetimbangan kimia!
Menurut seorang ahli kimia asal Perancis bernama Henry-Loius Le Chatelier, perubahan pergeseran kesetimbangan kimia dapat diprediksi. Hal tersebut disimpulkan dalam prinsip Le Chatelier.
Baca juga: Asas Le Chatelier tentang Pergeseran Kesetimbangan Reaksi Kimia
Kesetimbangan kimia dapat diprediksi bergeser ke arah produk ataupun ke arah reaktan, bergantung pada berbagai faktor.
Faktor-faktor yang memengaruhi kesetimbangan kimia adalah konsentrasi, suhu, tekanan, dan juga volume.
Konsentrasi
Dilansir dari Lumen Learning, menurut prinsip Le Chatelier menambahkan konsentrasi reaktan ke sistem akan menggeser kesetimbangan ke kanan atau ke arah produk. Artinya, reaksi kimia akan menghasilkan lebih banyak produk.
Sedangkan, jika konsentrasi produk yang ditambahkan ke sistem. Maka, kesetimbangan akan bergeser ke kiri atau ke arah reaktan. Sehingga, reaksi kimia akan menghasilkan lebih banyak reaktan.
Hal tersebut terjadi karena reaksi kimia yang sifatnya reversible akan mempertahankan kesetimbangannya.
Baca juga: Contoh Reaksi Kesetimbangan Kimia dalam Kehidupan Sehari-Hari
Suhu
Faktor yang memengaruhi kesetimbangan kimia selanjutnya adalah suhu. Perubahan suhu sistem dapat mengubah nilai konstanta kesetimbangan dan mengakibatkan pergeseran kesetimbangan.
Bagaimana suhu mengubah kesetimbangan, berkaitan erat dengan reaksi eksotermik dan reaksi endotermik.
Pada reaksi eksotermik, panas dihasilkan sebagai produk. Sedangkan, pada reaksi endotermik, panas diserap sebagai reaktan.
Sehingga sebagaimana dilansir dari Chemistry LibreTexts, meningkatkan suhu sama dengan menambahkan panas pada reaksi eksotermik dan endotermik.
Baca juga: Menentukan Pergeseran Kesetimbangan Reaksi dari Kc
Peningkatan suhu
Pada reaksi eksotermik, meningkatkan suhu sama dengan meningkatkan produk. Sehingga, reaksi kesetimbangan akan bergeser ke kiri dan menghasilkan lebih banyak reaktan.
Adapun pada reaksi endodermik, meningkatkan suhu sama dengan meningkatkan reaktan. Sehingga, reaksi kesetimbangan akan bergeser ke kanan dan menghasilkan lebih banyak produk.
Penurunan suhu
Pada reaksi eksotermik, menurunkan suhu sama dengan mengurangi jumlah produk. Sehingga, keretimbangan akan bergeser ke kanan.
Adapun pada reaksi endodermik, menurunkan…
-
![]()
Pengertian Kesetimbangan Dinamis
-
![]()
Asas Le Chatelier tentang Pergeseran Kesetimbangan Reaksi Kimia
-
![]()
Rumus Tetapan Kesetimbangan
-
![]()
Menghitung Reaksi Kesetimbangan dengan Tetapan Kc
-
![]()
Menghitung Reaksi Kesetimbangan Tetapan Kp
-
![]()
Hubungan Tetapan Kesetimbangan Kc dan Kp
-
![]()
Soal UAS Kimia: Konsep Kesetimbangan Dinamis
-
![]()
Kesetimbangan Kimia: Menentukan Amonia dalam Jumlah Maksimal
-
![]()
Contoh Reaksi Kesetimbangan Kimia dalam Kehidupan Sehari-Hari