Contoh Pasangan Asam dan Basa Konjugasi Bronsted Lowry
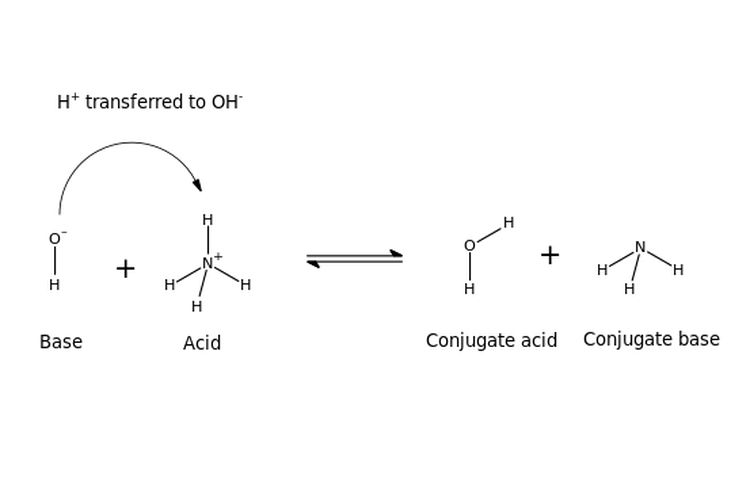
KOMPAS.com – Menurut teori Bronsted Lowry, asam adalah spesies yang dapat mendonorkan proton. Adapun, asam Bronsted memiliki pasangan basa konjugasinya. Berikut adalah contoh pasangan asam dan basa konjugasi Bronsted Lowry!
Dilansir dari Chemistry LibreTexts, basa konjugasi adalah asam yang telah mendonorkan atau kehilangan protonnya.
Artinya, asam melepaskan proton (H+) untuk mencapai kesetimbangan reaksi dan berubah menjadi basa konjugasi.
Baca juga: Teori Asam Basa: Pengertian Para Ahli dan Sifatnya
Dilansir dari Lumen Learning, basa konjugasi dari asam kuat bersifat sebagai basa yang sangat lemah.
Suatu asam dengan sifat keasaman tinggi (ka besar) akan menghasilkan basa konjugasi dengan sifat kebasaan yang rendah (kb kecil).
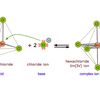
Misalnya, senyawa asam kuat hidrogen klodrida (HCl) yang dimasukkan ke dalam air (H2O).
HCL akan yang merupakan asam induk akan mendonorkan proton ke air dan membentuk basa konjugasi berupa Cl-.
Tidak seperti HCl yang memiliki sifat keasaman kuat, Cl- memiliki sifat kebasaan yang lemah.
Baca juga: Daftar Nama Asam-Basa Kuat dan Asam-Basa Lemah
Reaksi bersifat ireversibel atau bolak-balik. Di mana ion Cl- dapat kembali menerima proton dari H3O+ (air yang menerima proton) dan berubah kembali menjadi HCl.
Adapun, contoh pasangan asam dan basa konjugasi Bronsted Lowry adalah:
| Senyawa Asam | Basa Konjugasinya |
| HCL | CL- |
| HBr | Br- |
| HNO3 | NO3- |
| HC2H3O2 | C3H3O- |
| HI | I- |
| H2SO4 | HSO4- |
| H3PO4 | H2PO4- |
| CH3CO2H | CH3CO2- |
| H2S | HS- |
| CH3OH | CH3O- |
| H2O | OH- |
| HCN | CN- |
| H2SO3 | HSO3- |
| H2CO3 | HCO3- |
| C5H5NH+ | C5H5N |
Simak breaking news dan berita pilihan kami langsung di ponselmu. Pilih saluran andalanmu akses berita Kompas.com WhatsApp Channel : https://www.whatsapp.com/channel/0029VaFPbedBPzjZrk13HO3D. Pastikan kamu sudah install aplikasi WhatsApp ya.