Contoh sel volta dalam Kehidupan Sehari-hari
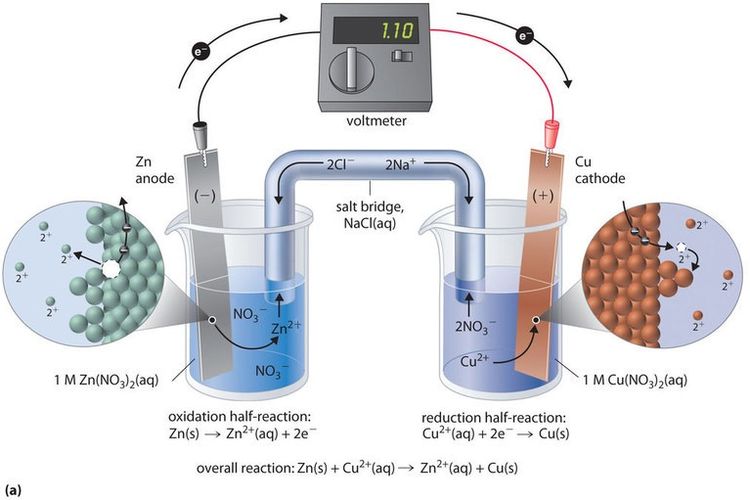
Ketika pengisian, maka gerakan ion litium berbalik, dari katode ke anode melalui larutan elektrolit.
Aki
Contoh sel volta dalam kehidupan sehari-hari adalah aki. Aki atau accumulator merupakan sel volta yang tersusun atar elektrode Pb (timbal) dan PbO (timbal (IV) oksida) dalam larutan H2SO4 sebagai larutan elektrolit.
Adanya larutan H2SO4 ini menyebabkan sel volta aki tidak memerlukan jembatan garam.
Pada aki, sel volta disusun atas beberapa pasang, dan tiap pasang dapat menghasilkan arus listrik sebesar 2V.
Baca juga: Kuat Arus Listrik: Pengertian, Satuan, dan Rumusnya
Aki motor biasanya sebesar 6V dan aki mobil biasanya sebesar 12V. Aki 12V terdiri dari 6 pasang sel volta yang disusun seri.
Aki dapat digunakan dan setelah habis dapat diisi ulang kembali, sehingga aki disebut sebagai sel sekunder.
Reaksi redoks yang terjadi pada aki meliputi reaksi penggunaan (reaksi pengosongan) dan reaksi pengisian.
- Reaksi pengosongan aki
-
- Anode (oksidasi): Pb(s)+HSO4-(aq)→PbSO4(s)+H+(aq)+2e-
- Katode (reduksi): PbO2(s)+HSO4-(aq)+3H+(aq)+2e-→PbSO4(s)+2H2O(l)
Reaksi total: Pb(s)+PBO2(s)+2HSO4-(aq)+2H+(aq)→2PbSO4(s)+2H2O(l)
Baca juga: Contoh Larutan Elektrolit dalam Kehidupan Sehari-hari
- Reaksi pengisian aki
-
- Anode (oksidasi): PbSO4(s)+2H2O(l)→PbO2(s)+HSO4-(aq)+3H+(aq)+2e-
- Katode (reduksi): PbSO4(s)+H+(aq)+2e-→Pb(s)+HSO4-(aq)
Reaksi total: 2PbSO4(s)+2H2O(l)→Pb(s)+PBO2(s)+2HSO4-(aq)+2H+(aq)
Sel bahan bakar
Sel bahan bakar merupakan bagian dari sel volta yang mirip dengan aki atau baterai, di mana bahan bakarnya diisi secara terus-menerus, sehingga dapat dipergunakan secara terus-menerus juga.
Bahan baku dari sel bahan bakar adalah gas hidrogen dan oksigen. Reaksi yang terjadi pada sel bahan bakar adalah:
- Anode: 2H2+4OH-→4H2O+4e-
- Katode: O2+2H2O+4e-→4OH-
Reaksi total: 2H2+O2→2H2O
Baca juga: Bahan Bakar Fosil: Minyak Bumi, Batu Bara, dan Gas Alam
Referensi:
- Sulastri, dan teman-teman. Kimia Dasar. 2017. Aceh: Syiah Kuala University Press.
- Sandra, Lovi dan teman-teman. Kimia Dasar. 2022. Padang: Global Eksekutif Teknologi.