Pengecualian dan Kegagalan Aturan Oktet

KOMPAS.com - Aturan oktet adalah suatu kaidah sederhana dalam kimia yang menyatakan bahwa atom dari kelompok unsur utama cenderung berikatan dengan atom lain.
Aturan oktet sangat berguna untuk memprediksi rumus kimia senyawa biner sederhana.
Aturan oktet dapat diterapkan pada unsur-unsur golongan utama. Suatu unsur dapat mencapai kestabilan dengan cara melepaskan elektron dan menerima atau menangkap elektron.
Namun, tidak semua unsur-unsur itu dapat mencapai aturan oktet.
Sehingga muncul, pengecualian aturan oktet dan juga aturan oktet sering dilanggar serta gagal memprediksi rumus kimia senyawa unsur transisi dan postransisi.
Baca juga: Aturan Oktet dalam Kimia
Untuk lebih jelasnya, simaknya pembahasan di bawah ini mengenai pengecualian dan kegagalan aturan oktet.
Pengecualian aturan oktet
Pengecualian aturan oktet dapat dibagi dalam tiga kelompok, yaitu:
- Senyawa yang tidak mencapai aturan oktet
- Senyawa dengan jumlah elektron valensi ganjil
- Senyawa yang melampaui aturan oktet
Senyawa yang tidak mencapai aturan oktet
Senyawa yang atom pusatnya mempunyai elektron valensi kurang dari 4 termasuk dalam kelompok ini.
Hal ini menyebabkan setelah semua elektron valensinya dipasangkan tetap belum mencapai oktet. Contohnya adalah BeCl2, BCl3, dan AlBr3.
Baca juga: Konfigurasi Elektron: Prinsip Aufbau, Larangan Pauli, dan Aturan Hund
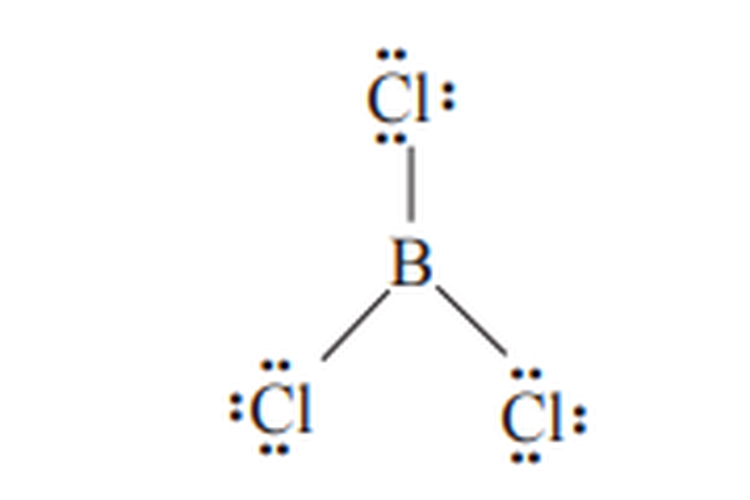 Senyawa yang Tidak Mencapai Aturan Oktet
Senyawa yang Tidak Mencapai Aturan Oktet(Atom b belum oktet)
Senyawa dengan jumlah elektron valensi ganjil
Contohnya adalah NO2, yang mempunyai elektron valensi (5 + 6 + 6) =17. Kemungkinan rumus Lewis untuk NO2 sebagai berikut.
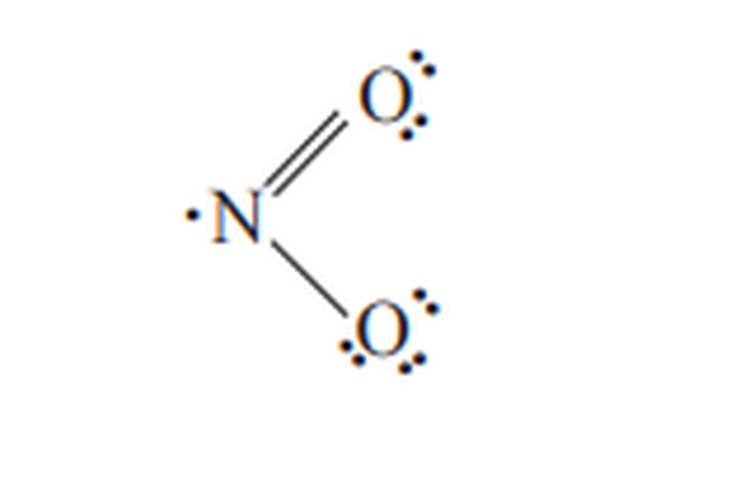 Senyawa dengan Jumlah Elektron Valensi Ganjil
Senyawa dengan Jumlah Elektron Valensi GanjilSenyawa yang melampaui aturan oktet
Ini terjadi pada unsur-unsur periode 3 atau lebih yang dapat menampung lebih dari 8 elektron pada kulit terluarnya (ingat, kulit M dapat menampung hingga 18 elektron).
Beberapa contoh senyawa yang melampaui aturan oktet adalah PCl5, SF6, ClF3, IF7, dan SbCl5.
Baca juga: 3 Partikel Penyusun Materi: Atom, Molekul, dan Ion
Perhatikan rumus Lewis dari PCl5, SF6, dan ClF3 berikut ini.
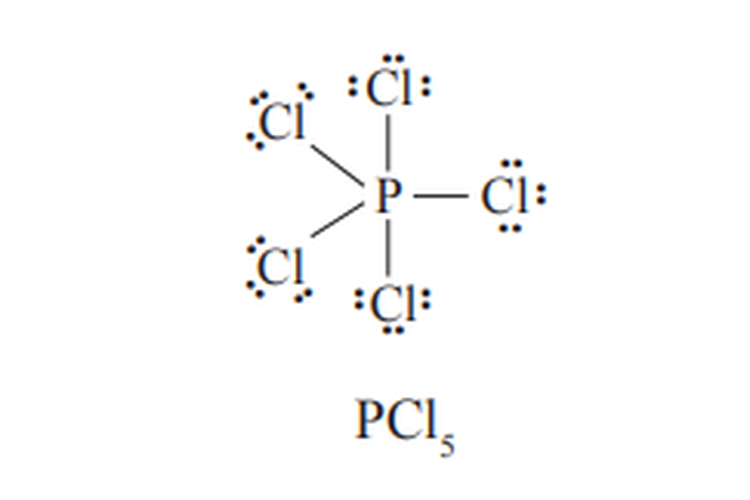 Senyawa yang Melampaui Aturan Oktet
Senyawa yang Melampaui Aturan Oktet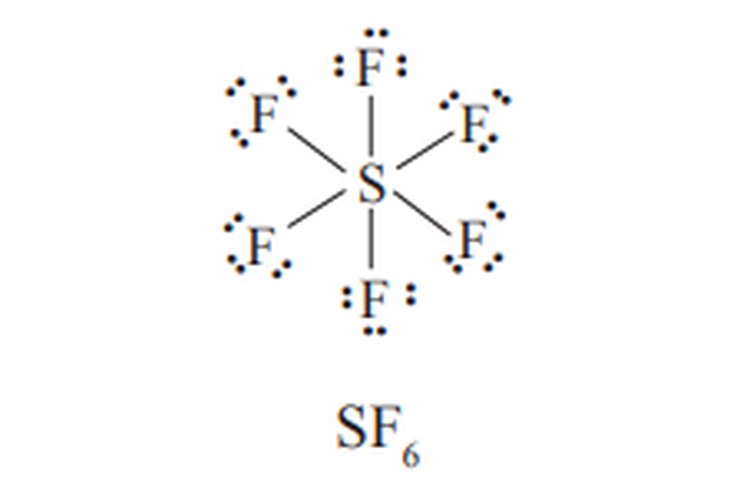 Senyawa yang Melampaui Aturan Oktet
Senyawa yang Melampaui Aturan Oktet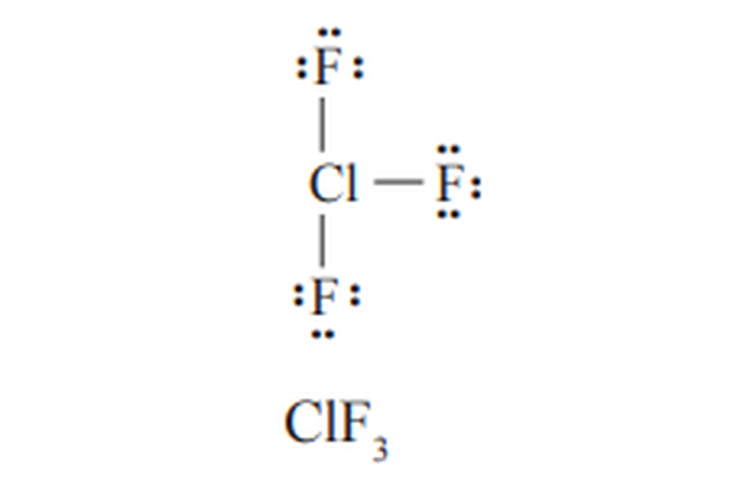 Senyawa yang Melampaui Aturan Oktet
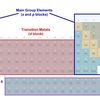
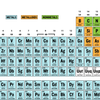
Senyawa yang Melampaui Aturan OktetKegagalan aturan oktet
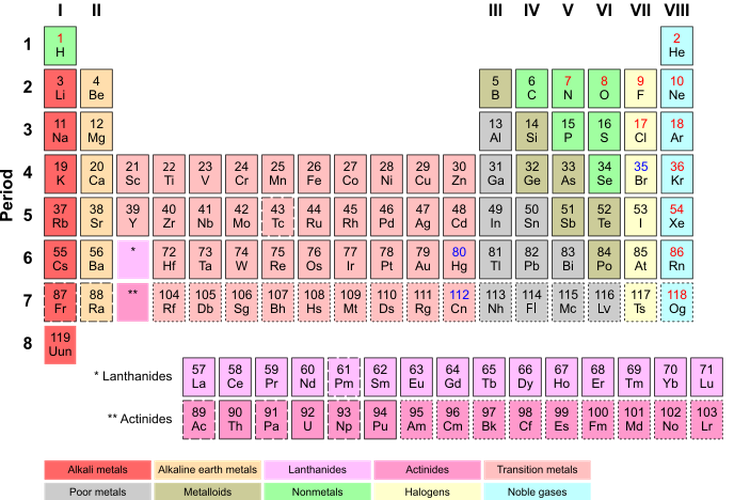 Gambar tabel periodik
Gambar tabel periodikBaca juga: Perbedaan Sifat Unsur Golongan Transisi dengan Unsur Golongan Utama