Hidrolisis Garam: Pengertian, Jenis, dan Rumusnya

KOMPAS.com - Garam adalah kata yang sangat akrab di dengar. Namun tahukah kamu bahwa ada banyak jenis garam di dunia? Garam adalah senyawa ionik yang terbentuk akibat reaksi netralisasi asam dan basa.
Kebalikan reaksi netralisasi asam basa adalah hidrolisis garam. Hidrolisis berasal dari bahasa Yunani “hydro” yang berarti air dan “lysis” yang berarti lepas atau penguraian.
Hidrolisis garam dapat diartikan sebagai reaksi reversible penguraian garam oleh air. Sehingga, hidrolisis garam adalah reaksi antara salah satu ion-ion garam (kation atau anion) dengan air dan membentuk larutan bersifat asam atau basa.
Sifat asam atau basa larutan yang dihasilkan hidrolisis garam bergantung pada jenis asam basa yang membentuk garam tersebut.
Baca juga: Hukum Kekekalan Energi: Pengertian, Rumus, dan Penerapannya
Misalnya garam yang terbentuk dari asam kuat dan basa kuat, garam yang terbentuk dari asam kuat dan basa lemah, garam yang terbentuk dari asam lemah dan basa kuat, serta garam yang terbentuk dari asam lemah dan basa lemah.
Garam dari asam kuat dan basa kuat
Dilansir dari The Fact Factor, garam yang terbentuk dari asam kuat dan basa kuat tidak akan mengalami hidrolisis karena baik kation maupun anionnya tidak bereaksi dengan air.
Misalnya garam natrium klorida (NaCl) yang terbentuk dari asam kuat dan basa kuat, yaitu asam klorida (HCl) dan natrium hidroksida (NaOH).
 Ionisasi natrium klorida
Ionisasi natrium klorida
Dari reaksi terlihat ion yang terbentuk saat garam NaCl dilarutkan dalam air adalah OH- dan H+. keduanya akan saling menetralkan, dan tidak bereaksi dengan air.
Dengan kata lain garam NaCl hanya terionisasi dan tidak terhidrolisis, sehingga larutan yang dihasilkannya bersifat netral (pH=7).
Garam dari asam kuat dan basa lemah
Garam dari asam kuat dan basa lemah akan mengalami hidrolisis sebagian. Misalnya ammonium klorida (NH4Cl) yang terbentuk dari asam kuat dan basa lemah, yaitu asam klorida (HCl) dan ammonia (NH3). Amonia akan mengalami ionisasi terurai menjadi ion NH4+ dan Cl-.
Baca juga: Senyawa Hidrokarbon: Pengertian, Rumus, Golongan, dan Contohnya
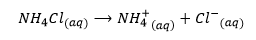 Ionisasi amonium klorida
Ionisasi amonium klorida
Perlu diingat bahwa ion Cl- dari asam kuat HCl tidak akan terhidrolisis oleh air, maka hanya ion NH4+ yang akan bereaksi dengan air dan meningkatkan konsentrasi ion hidronium.
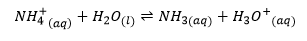 Hidrolisis amonium klorida
Hidrolisis amonium klorida
Hidrolisis garam ammonium klorida akan mengasilkan larutan asam dengan pH di bawah 7. Dari persamaan tersebut, kita dapat menghitung derajat hidrolisisnya untuk menghitung pH larutannya.
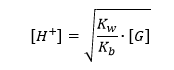 Rumus derajat hidrolisis garam dari asam kuat dan basa lemah
Rumus derajat hidrolisis garam dari asam kuat dan basa lemah
Keteragan:
H : derajat hidrolisis
Kw : konstanta ionisasi air (1x10^-14)
Kb : konstanta basa
[G] : konsentrasi kation garam
Garam dari asam lemah dan basa kuat
Garam dari asam lemah dan basa kuat jika di hidrolisis akan menghasilkan larutan basa. Misalnya garam natrium flurida (NaF) yang terbentuk dari asam lemah flurida (HF) dan basa kuat natrium hidroksida (NaOH).
 Ionisasi natrium flurida
Ionisasi natrium flurida
Kation Na+ dari basa kuat natrium hidrokida tidak akan terhidrolisis. Dilansir dari Lumen Learning, sedangkan anion F- adalah basa konjugasi HF yang akan menerima proton dari air (terhidrolisis).
Baca juga: Akor: Pengertian, Fungsi, Rumus dan Simbolnya
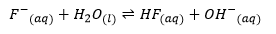 Hidrolisis natrium flurida
Hidrolisis natrium flurida
Saat anion (F-) terhidrolisis dengan air, maka terbentuk ion OH- yang membuat larutan bersifat asam dengan pH lebih besar dari 7. Derajat hidrolisisnya dapat dicari dengan rumus:
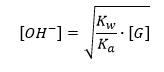 Rumus derajat hidrolisis garam dari asam lemah dan basa kuat
Rumus derajat hidrolisis garam dari asam lemah dan basa kuat
Keterangan: