Teori Atom Niels Bohr: Isi, Kelebihan, dan Kelemahannya

KOMPAS.com - Teori atom Niels Bohr dikembangkan oleh seorang fisikawan asal Denmark, Niels Bohr, pada 1913.
Pengembangan konsep ini berangkat dari teori atom milik Ernest Rutherford yang dikemukakan pada 1911.
Isi teori atom Niels Bohr
Dikutip dari Buku Ajar Teori Dasar Listrik dan Elektronika (2022) karya Muhammad Naim, secara garis besar, isi teori atom Niels Bohr adalah:
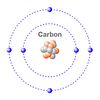
"Elektron yang bermuatan negatif berputar mengelilingi atom bermuatan positif pada jalur lintasannya sendiri."
Menurut Sulaiman dalam buku Perubahan Fisik dan Sifat Benda (2019), jika dirinci, berikut isi teori atom Niels Bohr:
- Elektron mengorbit inti atom pada lintasan tertentu dan khas
- Atom yang berbeda akan memiliki struktur orbit elektron yang berbeda pula
- Atom dapat menyerap atau melepaskan energi
- Jika atom menyerap energi, elektronnya akan melompat ke tingkatan orbit yang lebih tinggi
- Apabila atom melepaskan energi, elektron akan turun ke tingkatan orbit yang lebih rendah
- Ketika atom melepaskan energi, foton cahaya akan dipancarkan. Besaran energi yang hilang dari atom sama besarnya dengan energi kuantum cahaya yang terpancar.
Baca juga: 3 Partikel Penyusun Materi: Atom, Molekul, dan Ion
Kelebihan teori atom Niels Bohr
Dilansir dari Buku Ajar Kimia 1 (2022) oleh Maris Kurniawati, berikut kelebihan teori atom Niels Bohr:
- Menjawab kelemahan (kekurangan) teori atom Rutherford dengan mengaplikasikan teori kuantum
- Menerangkan dengan jelas garis spektrum pancaran (emisi) atau serapan (absorpsi) dari atom hidrogen.
Kelemahan teori atom Niels Bohr
Tidak hanya memiliki kelebihan, teori atom ini juga memiliki sejumlah kelemahan. Berikut dua kelemahan teori atom Niels Bohr:
- Ada penyimpangan untuk atom yang lebih besar ketimbang hidrogen
- Tidak dapat menerangkan efek Zaeman yang terjadi ketika atom ditempatkan pada medan magnet.
Kelemahan lainnya, yakni Bohr hanya menjelaskan spektrum atom hidrogen. Tetapi tidak menggambarkan spektrum atom dengan jumlah elektron yang lebih banyak.
Baca juga: Teori Atom Chadwick: Penemuan Neutron dan Model Atomnya
Simak breaking news dan berita pilihan kami langsung di ponselmu. Pilih saluran andalanmu akses berita Kompas.com WhatsApp Channel : https://www.whatsapp.com/channel/0029VaFPbedBPzjZrk13HO3D. Pastikan kamu sudah install aplikasi WhatsApp ya.