Apa Itu Halogenasi?

KOMPAS.com - Halogen dalam tabel periodik adalah golongan 17 yang terdiri dari unsur-unsur non logam dan berada disebelah kiri gas mulia. Unsur-unsur tersebut terdiri dari fluor (F), klor (Cl), brom (Br), dan yodium (I).
Gas halogen memiliki tujuh elektron valensi sehingga membutuhkan 1 elektron untuk memenuhi aturan oktet. Hal tersebut membuat unsur halogen sangat reaktif sehingga mudah membentuk reaksi halogenasi.
Dilansir dari Encyclopedia Britannica, halogenasi adalah reaksi kimia penggantian satu atau lebih atom hidrogen dengan atom dari unsur halogen.
Reaksi halogenasi terdiri dari dua jenis reaksi, yaitu reaksi subtitusi dan reaksi adisi. Untuk lebih memahaminya, yuk kita simak contoh reaksi halogenasi di bawah ini:
Baca juga: Contoh Reaksi Reduksi
- Klorinasi Metana
Klorinasi metana adalah reaksi eksotermik subtitusi gas klor ke dalam atom metana untuk menggantikan keberadaan atom hidrogen. Dilansir dari Chemistry LibreTexts, dalam reaksi halogenasi tersebut ikatan CH dan CL-CL terputus dan tergantikan dengan ikatan kovalen C-Cl serta H-Cl.
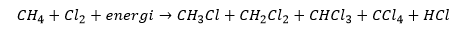 Reaksi klorinasi metana
Reaksi klorinasi metana
Dari persamaan reaksi terlihat bahwa metana bereaksi dengan klorin menghasilkan metil klorida sebagai produk utama, dan diklorometana, klorofom, serta tetraklorometana sebagai produk sampingan.
- Halogenasi Alkena
Brominasi merupakan reaksi adisi brom (Br2) ke dalam ikatan rangkap alkena. Reaksi adisi dimulai dengan ikatan rangkap alkena yang mempolarisasi ikatan bromin menjadi Br-Br.
Muatan postif Br kemudian akan bertindak sebagai elektrofil yang kemudian berikatan dengan dua karbon alkena.
Baca juga: Reaksi Eksotermal Pembentukan Nitrogen Dioksida (NO2)
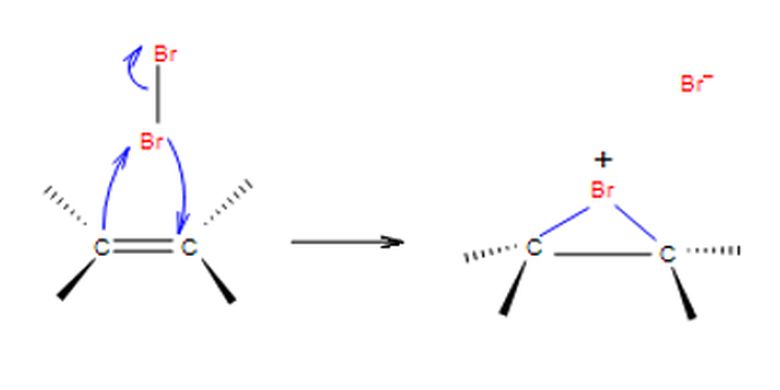 Pembentukan ion siklik alkena
Pembentukan ion siklik alkenaIkatan tersebut membentuk ion siklik alkena. Kemudian muatan negatif bromida yang sempat terputus karena pembelahan heterolitik akan berikatan dengan salah satu karbon alkena.
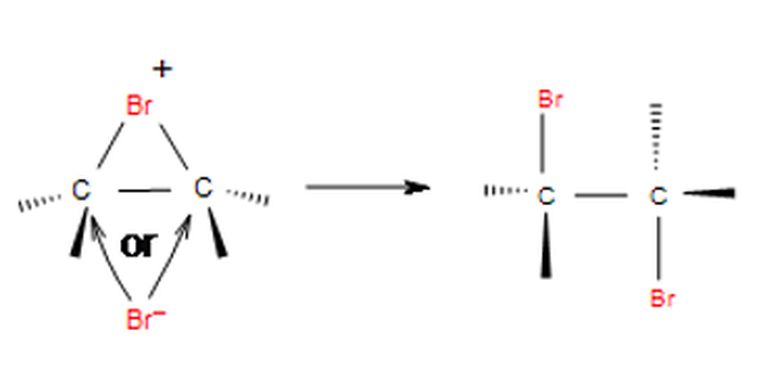 Pembentukan dihalida vicinal
Pembentukan dihalida vicinalReaksi tersebut menghasilkan dua halogen dengan cincin terbuka dengan gugus halide yang terikat pada karbon alkena. Dua halogen tersebut merupakan senyawa organik halida yang disebut dengan dihalida vicinal.
Dilansir dari Chemguide, halogenasi alkena paling cocok menggunakan bromin dibanding dengan unsur halogen lainnya.
Hal tersebut karena klorin bereaksi lebih cepat namun menghasilkan kimia yang serupa, yodium juga menghasilkan kimia yang serupa namun jauh lebih lambat, sementara fluor terlalu reaktif sehingga bisa menyebabkan ledakan yang tidak diinginkan.
- Halogenasi Benzena
Reaksi halogenasi juga dapat terjadi pada senyawa benzena secara subtitusi. Namun halogenasi benzena tidak dapat terjadi secara spontan sehingga halogen harus diaktifkan oleh katalis.
Baca juga: Menentukan Pergeseran Kesetimbangan Reaksi dari Kc
Contoh katalis halogenasi benzena adalah besi atau asam lewis eperti alumunium bromide dan aluminum klorida.
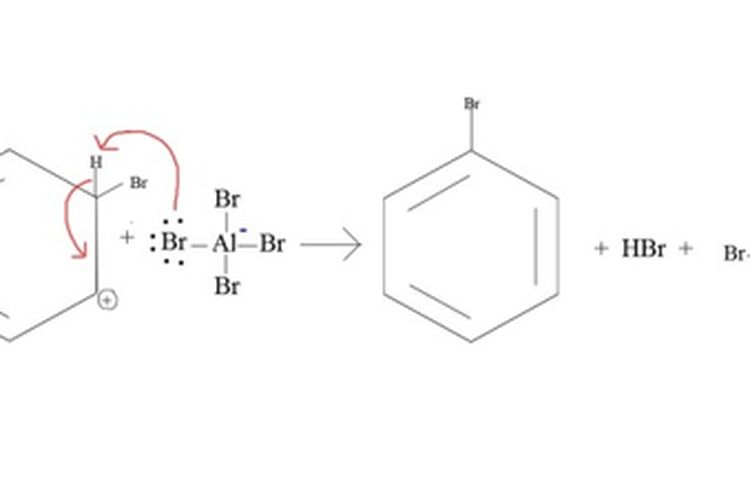
Unsur halogen yang berikatan dengan katali akan menghasilkan elektrofil. Misalnya bromin (Br2) yang menggunakan aluminum bromide untuk menjadi katalis akan membentuk ikatan halogen-halogen yang elektrofilik yaitu Br-Br-AlBr3.
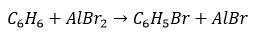 Persamaan reaksi halogenasi benzena oleh bromin
Persamaan reaksi halogenasi benzena oleh bromin
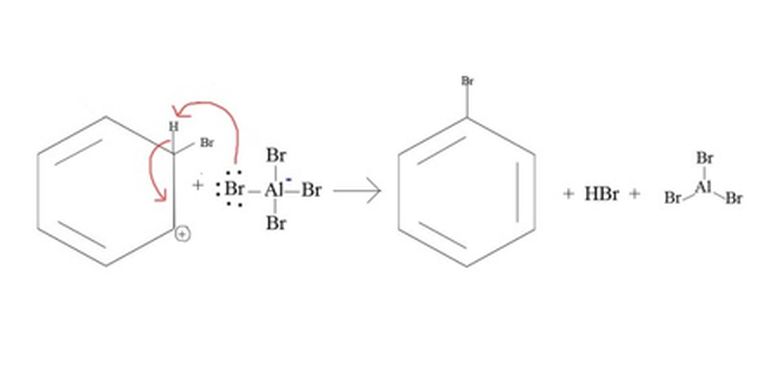 Halogenasi benzena yang dibantu oleh katalis
Halogenasi benzena yang dibantu oleh katalisDalam reaksi tersebut atom hidrogen dalam benzena digantikan oleh elektrofilik AlBr2. Reaksi halogenasi aromatik tersebut bersifat eksotermik dan alumunium bromide sebagai katalis tidak akan dikonsumsi sama sekali dalam reaksi.
Simak breaking news dan berita pilihan kami langsung di ponselmu. Pilih saluran andalanmu akses berita Kompas.com WhatsApp Channel : https://www.whatsapp.com/channel/0029VaFPbedBPzjZrk13HO3D. Pastikan kamu sudah install aplikasi WhatsApp ya.