4 Hukum Dasar Kimia
Air dibentuk oleh dua unsur yaitu unsur hidrogen dan oksigen. Materi memiliki massa, termasuk hidrogen dan oksigen.
Ahli kimia dari Perancis, Joseph Louis Proust mencoba menggabungkan hidrogen dan oksigen untuk membentuk air.
Baca juga: Persamaan Reaksi dan Penyetaraannya
Didapatkan bahwa setiap satu gas hidrogen bereaksi dengan delapan gas oksigen, menghasilkan sembilan gass air.
Hal ini membuktikan bahwa massa hidrogen dan massa oksigen yang terkandung dalam air memiliki perbandingan tetap 1:8. Berapapun banyaknya air yang terbentuk.
Dari percobaan yang dilakukannya, hukum perbandingan tetap, berbunyi:
"Perbandingan massa unsur-unsur penyusun suatu senyawa selalu tetap"
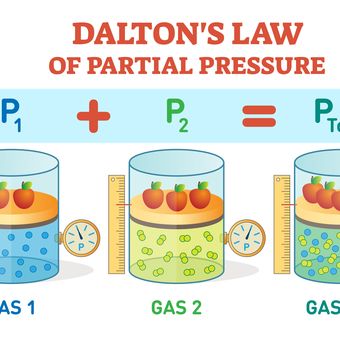 Ilustrasi hukum daltonHukum perbandingan berganda (Hukum Dalton)
Ilustrasi hukum daltonHukum perbandingan berganda (Hukum Dalton)
 Ilustrasi hukum dalton
Ilustrasi hukum daltonKomposisi kimia ditunjukkan oleh rumus kimianya. Dalam senyawam seperti air, ada dua unsru bergabung dan masing-nmasing memberikan sejumlah atom untuk membentuk senyawa.
Dari dua unsur dapat dibentuk beberapa senyawa dengan perbandingan berbeda-beda.
Misalnya belerang dengan oksigen dapat membentuk senyawa SO2 dan SO3. Dari unsur hidrogen dan oksigen daoat dibentuk senyawa H2O dan H2O2.
Baca juga: Pengertian Gaya, Rumus, dan Macamnya
Dalton menyelidiki perbandingan unsur tersebut pada setiap senyawa dan mendaoatkan suatu poloa teratur.
Pola tersebut dinyatakan sebagai hukum perbandingan berganda, yaitu:
"Apabila dua unsur dapat membentuk lebih dari satu senyawa, massa salah satu unsur tersebut tetap (sama), maka perbandingan massa unsur yang lain dalam senyawa-senyawa tersebut merupakan bilangan bulat dan sederhana"
Hukum perbandingan volume (Gay Lussac)
Pada awalnya para ilmuwan menemukan bahwa gas hidrogen dapat bereaksi dengan gas oksigen membentuk air.
Perbandingan volume gass hidrogen dan oksigen dalam reaksi tersebut tetap, yakni 2:1.
Kemudian di tahun 1808, ilmuwan Perancis, Joseph Gay Lussac berhasil melakukan percobaan mengenai volume gas yang terlibat berbagai reaksi dengan menggunakan berbagai macam gas.