KOMPAS.com - Bagaimana menentukan rumus molekul senyawa? Jika anda belum bisa menentukan nya. Berikut tersaji dua soal tentang penentuan rumus molekul senyawa beserta pembahasan nya:
1. Suatu Kristal barium klorida didalamnya mengandung 25% air. Jika Mr Kristal barium adalah 208 dan Mr air adalah 18, tentukanlah rumus molekul Kristal tersebut!
Jawaban:
Kristal barium yang mengandung air dinamakan dengan senyawa hidrat. Dilansir dari Encyclopaedia Britannica, senyawa hidrat adalah senyawa yang mengandung molekul air H2O dan pada umumnya berbentuk padatan Kristal.
Untuk mengetahui rumus molekul Kristal hidrat Barium klorida, ikuti langkah-langkah berikut:
- Tentukan massa barium klorida dan massa air:
Misalkan massa Kristal hidrat Barium klorida adalah 100 gram, dan 25% nya adalah air berarti:
Massa Barium klorida = 75% x 100 gram = 75 gram
Massa air = 25% x 100 gram = 25 gram
- Tentukan perbandingan jumlah mol Barium klorida dan air pada Kristal hidrat:
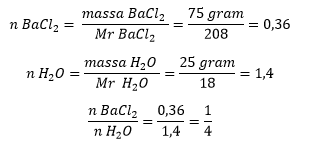 Perhitungan perbandingan mol Barium klorida dan air
Perhitungan perbandingan mol Barium klorida dan air
Baca juga: Cara Menentukan Rumus Molekul dalam Senyawa
Perbandingan sederhana jumlah mol Barium klorida dan air adalah 1:4 yang berarti 1 molekul Barium klorida akan bereaksi dengan 4 molekul air, sehingga rumus molekulnya adalah:
 Rumus molekul kristal hidrat barium klorida
Rumus molekul kristal hidrat barium klorida
 Ilustrasi kimia
Ilustrasi kimia2. Dalam suatu percobaan ditemukan bahwa suatu oksida nitrogen mengandung 36,37% massa oksigen. Jika Ar N adalah 14 dan Ar O adalah 16, tentukanlah apa rumus molekul oksida nitrogen tersebut!
Jawaban:
- Anggaplah massa oksida nitrogen tersebut adalah 100 gram untuk memudahkan pekerjaan, lalu tentukan massa dari nitrogen dan oksigen:
Massa Oksigen = 36,37% x 100 gram = 36,37 gram
Massa Nitrogen = 63,63% x 100 gram = 63,63 gram
- Tentukan perbendingan mol kedua zat pereaksinya:
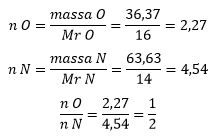 Perhitungan perbandingan mol Oksigen dan Natrium
Perhitungan perbandingan mol Oksigen dan Natrium
Perbandingan jumlah mol oksigen dan nitrogen adalah 1:2 yang berarti 1 molekul oksigen bereaksi dengan 2 molekul nitrogen dan rumus molekulnya adalah:
 Rumus molekul Nitrogen dioksida
Rumus molekul Nitrogen dioksida
Baca juga: Perbedaan Rumus Molekul dan Rumus Empiris
Simak breaking news dan berita pilihan kami langsung di ponselmu. Pilih saluran andalanmu akses berita Kompas.com WhatsApp Channel : https://www.whatsapp.com/channel/0029VaFPbedBPzjZrk13HO3D. Pastikan kamu sudah install aplikasi WhatsApp ya.