Rumus Kimia dan Tatanama Senyawa
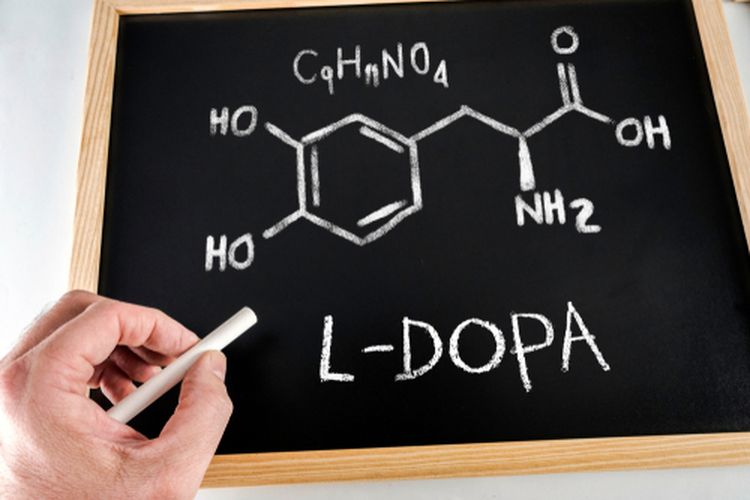
KOMPAS.com - Pernahkah kalian melihat pembakaran kayu? Pembakaran kayu merupakan salah satu contoh dari reaksi kimia.
Kayu yang terbakar mengalami perubahan wujud. Hasil dari pembakaran, yaitu abu, gas CO2, dan uap air tidak bisa kembali lagi menjadi kayu.
Dilansir dari situs Kementerian Pendidikan dan Kebudayaan Republik Indonesia, simbol yang digunakan untuk mengenali suatu molekul dinamakan rumus kimia.
Penggunaan rumus kimia erat kaitannya dengan tatanama senyawa.
Rumus kimia
Rumus kimia zat menyatakan jenis dan jumlah relatif atom-atom yang terdapat dalam zat.
Angka yang menyatakan jumlah atom suatu unsur dalam rumus kimia disebut angka indeks.
Baca juga: Pengertian Gaya, Rumus, dan Macamnya
Rumus kimia zata terbagi menjadi dua, yaitu:
Rumus molekul
Rumus molekul adalah rumus yang menyatakan jumlah atom-atom dari unsur yang menyusun satu molekul senyawa.
Sehingga rumus molekul menyatakan susunan dari molekul zat.
Misalnya, rumus molekul air adalah H2O, artinya dalam satu molekul air terdapat dua atom hidrogen dan satu atom oksigen.
Rumus empiris
Rumus empiris adalah rumus yang menyatakan perbandingan terkecil atom-atom dari unsur yang menyusun suatu senyawa.
Rumus kimia senyawa ion merupakan rumus empiris.
Misalnya, natrium klorida merupakan senyawa ion yang terdiri atas ion Na+ dan ion Cl- dengan perbandingan 1:1. Rumus kimia natrium klorida adalah NaCl.
Pada kondisi lain, sebagian uinsur-unsur ada yang membentuk molekul-molekul. Rumus kimia unsur-unsur ini tidak digambarkan hanya dengan lambang unsurnya, melainkan unsur beserta jumlah atom yang terbentuk.
Misalnya, rumus kimia gas oksigen, yaitu O2, artinya rumus kimia gas oksigen terdiri atas molekul-molekul oksigen yang dibangun oleh dua atom oksigen.
Semua senyawa memiliki rumus empiris. Senyawa molekul memiliki rumus molekul selain rumus empiris.
Pada banyak senyawa, rumus molekul sama dengan rumus empirisnya. Senyawa ion hanya memiliki rumus empiris.
Baca juga: Rumus Skala Peta, Menghitung Jarak Sebenarnya dari Jarak di Peta
Sehingga, semua senyawa yang memiliki rumus molekul, pasti memiliki rumus empiris. Sedangkan yang memiliki rumus empiris, belum tentu memiliki rumus molekul.
Tatanama senyawa
Nama ilmiah suatu unsur memiliki asal-usul yang bermacam-macam.
Ada yang didasarkan pada warna unsur, salah satu sifat unsur yang bersangkutan, atau nama seorang ilmuwan yang sangat berjasa.
Untuk mencegah timbulnya perdebatan mengenai nama, Persatuan Kimia Murni dan Kimia Terapan atau IUPAC menetapkan aturan penamaan dan pemberian lambang bagi unsur temuan baru.
Berikut aturannya:
- Nama berakhir dengan ium, baik unsur logam atau nonlogam.
- Nama itu didasarkan pada nomor ataom unsur, yaitu rangkaian akar kata yang menyatakan nomor atomnya.
| 0 = nil | 4 = quad | 8 = okt |
| 1 = un | 5 = pent | 9 = enn |
| 2 = bi | 6 = hex | |
| 3 = tri | 7 = sept |
- Lambang unsur (tanda atom) terdiri dari tiga huruf yakni rangkaian huruf awal dari akar yang menyatakan nomor atom unsur tersebut.
Sistem penamaan
Namun, aturan penamaan IUPAC jarang digunakan. Ada beberapa sistem penamaan yang didasarkan pada rumus kimia senyawa, yaitu:
Tatanama senyawa biner
Senyawa biner adalah senyawa yang hanya terbentuk dari dua macam unsur yang berbeda. Biasanya terdiri dari unsur logam dan nonlogam.
Pada senyawa biner, unsur logam sebagai kation (ion positif) dan unsur nonlogam sebagai anion (ion negatif).
Baca juga: Sifat Kimia dan Fisik Air Laut
Berikut cirinya:
- Unsur yang berada di depan disebut sesuai dengan nama unsur tersebut.
- Unsur yang berada di belakang disebut sesuai dengan nama unsur tersebut dengan menambahkan akhiran-ida.
- Jumlah atom unsur disebut dengan menggunakan angka Latin, jika diperlukan.
Contohnya:
NO = nitrogen monoksida
NO2 = nitrogen dioksida
AlCl = alumunium klorida
 Ilustrasi rumus kimiaSenyawa biner kedua-duanya nonlogam
Ilustrasi rumus kimiaSenyawa biner kedua-duanya nonlogam
 Ilustrasi rumus kimia
Ilustrasi rumus kimiaSenyawa biner kedua-duanya nonlogam merupakan senyawa yang tersusun atas molekul-molekul, bukan ion-ion.
Penamaan ditandai dengan awalan angkan Yunani yang menyatakan jumlah atom nonlogam, kemudian diakhir dengan jumlah atom nonlogam diakhiri dengan akhiran -ida.
Awalan angka Yunani, yaitu
Mono = 1
Di = 2
Tri = 3
Tetra = 4
Penta = 5
Heksa = 6
Hepta = 7
Okta = 8
Nona = 9
Deka = 10
Contoh:
CO = Karbon monoksida
N2O5 = Dioksida pentaoksida
PCl5 = Fosfor pentaklorida
Senyawa yang tersusun atas ion-ion poliaton
Ion-ion dibedakan menjadi ion atom tunggal (ion monoatom) dan ion yang tersusun atas gabungan beberapa unsur yang disebut ion-ion poliatom.
Cara pemberian nama senyawa yang tersusun atas kation dan anion poliatomik yaitu, nama logam kation diikuti nama anionnya.
Baca juga: Larutan Elektrolit dan Ikatan Kimia
Khusus untuk logam golongan B disesuaikan dengan bilangan oksida unsur tersebut dalam senyawanya.
Contoh:
NH4Cl = amonium klorida
NaNO3 = natrium nitrat
MgSO4 = magnesium sulfat
Hal-hal yang perlu diperhatikan dalam pemberian nama senyawa ion poliatomik sebagai berikut:
- Kebanyakan ion poliatom bermuatan negatif kecuali ion amonium.
- Hampir seluruh ion poliatom mengandung oksigen, kecuali CN- dan NH4+.
- Suatu senyawa bersifat netral. Oleh karena itu, apabila suatu senyawa belum netral, ion-ion yang berbeda muatannya harus disamakan terlebih dahulu dengan menambahkan angka indeks.
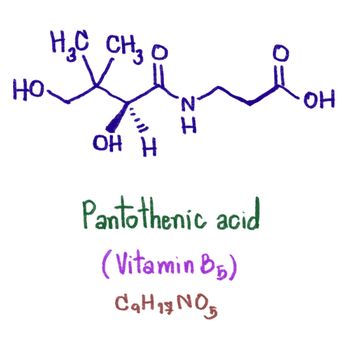 IlustrasiTatanama senyawa asam
IlustrasiTatanama senyawa asam
 Ilustrasi
IlustrasiAsam adalah zat yang jika dilarutkan di dalam air akan terlarut dan terurai menghasilkan ion hidrogen (H+) dan ion negatif.
Semua asam diawali dengan hidrogen kecuali asam organik dan air.
Pada umumnya asam merupakan senyawa biner yang mengandung hidrogen, oksigen, dan unsur nonlogam.
Semua asan dinamai dengan awalan asam yang diikuti nama ion negatifnya.
Tatanama senyawa hidrat
Beberapa senyawa yang berwujud kristal mampu mengikat air dari udara atau bersifat higroskopis, sehingga kristal senyawa tersebut mengandung air kristal.
Senyawa yang mengandung air kristal disebut hidrat. Kristal hidrat tidak berair karena molekul air terkurung rapat dalam kristal senyawa.
Senyawa hidrat dinamai dengan menambahkan awalan angka Yunani yang menyatakan banyaknya air kristal hidrat di akhir nama senyawa tersebut.
Baca juga: Memahami Proses dan Reaksi Kimia Fotosintesis
Simak breaking news dan berita pilihan kami langsung di ponselmu. Pilih saluran andalanmu akses berita Kompas.com WhatsApp Channel : https://www.whatsapp.com/channel/0029VaFPbedBPzjZrk13HO3D. Pastikan kamu sudah install aplikasi WhatsApp ya.