Aturan Oktet dalam Kimia

KOMPAS.com - Pernahkah kamu mendengar aturan oktet dalam ilmu kimia? Unsur akan stabil jika memiliki elektron valensi 8. Pada materi kali ini kita akan membahas tentang aturan oktet dan mengapa harus angka 8.
Setiap unsur di Bumi tersusun dari proton dan neutron pada inti atom dan elektron pada kulit atom. Elektron valensi atau elektron pada kulit terluar atomlah yang menentukan apakah suatu unsur stabil atau tidak.
Dilansir dari Chemistry LibreTexts, aturan oktet menyatakan bahwa atom cenderung bereaksi dengan unsur lainnya untuk membentuk 8 elektron valensi dan berubah menjadi stabil. Delapan buah elektron valensi dianggap stabil karena kulit terluar atom tersebut terisi penuh.
Saat kulit elektron terluar terisi penuh, unsur tersebut akan sulit untuk melepas maupun menerima elektron dari lingkungan sehingga stabil dan tidak mudah bereaksi.
Baca juga: Menghitung Reaksi antara Asam Nitrat dan Gas Amonia
Untuk atom yang memiliki elektron valensi lebih atau kurang dari 8, maka atom tersebut akan berikatan dengan atom lain.
Contohnya adalah karbon (C) yang berikatan dengan 2 atom oksigen (O) untuk memenuhi aturan oktet. Karbon memiliki elektron valensi 4 dan oksigen memiliki elektron valensi 6.
 Molekul karbon dioksida (CO2)
Molekul karbon dioksida (CO2)
Terlihat pada gambar bahwa C berikan dengan 2 O. Sehingga O memiliki tambahan 2 elektron valensi dari C, dan C memiliki 4 tambahan elektron valensi dari kedua atom O.
Contoh Soal:
Gas mulia yang memiliki susunan elektron valensi tidak sesuai aturan oktet adalah…
Jawaban:
Ada enam unsur dalam golongan gas mulia, yaitu helium (He), neon (Ne), argon (Ar), kripton (Kr), xenon (Xe), dan radon (Rn). Untuk mengetahui apakah unsur-unsur tersebut memenuhi aturan oktet, kita harus menentukan konfigurasi elektronnya:
[He]: 2
[Ne]: 2 8
[Ar]: 2 8 8
[Kr]: 2 8 18 8
[Xe]: 2 8 18 18 8
[Rn]: 2 8 18 32 18 8
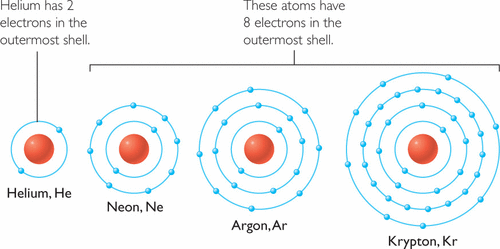 Lintasan elektron pada unsur-unsur gas mulia
Lintasan elektron pada unsur-unsur gas mulia
Hanya helium unsur gas mulia yang tidak mengikuti akturan oktet karena elektron valensinya bukanlah 8, melainkan mengikuti aturan duplet.
Dilansir dari Brilliant, helium mengikuti aturan duplet dimana atomnya dapat stabil dengan hanya 2 elektron pada kulitnya. Hal ini karena helium hanya memiliki satu kulit elektron yang hanya dapat menampung 2 elektron.
Simak breaking news dan berita pilihan kami langsung di ponselmu. Pilih saluran andalanmu akses berita Kompas.com WhatsApp Channel : https://www.whatsapp.com/channel/0029VaFPbedBPzjZrk13HO3D. Pastikan kamu sudah install aplikasi WhatsApp ya.