Teori Kinetik Gas dan Hukumnya
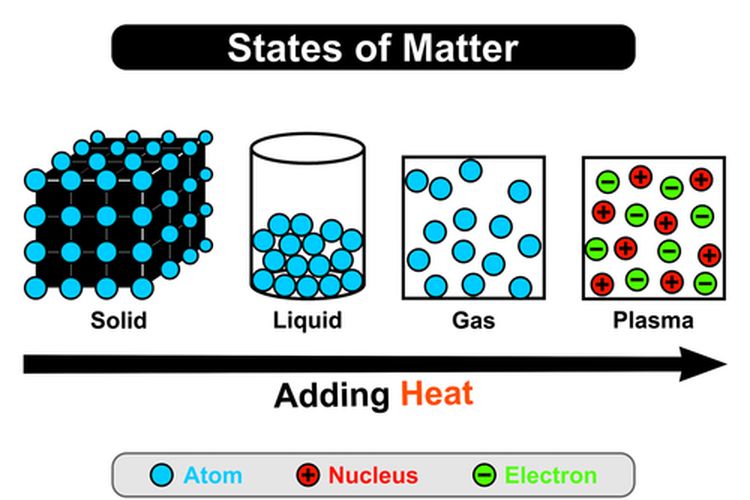
KOMPAS.com - Teori kinetik pada gas berupaya menjelaskan sifat-sifat makroscopik gas, seperti tekanan, suhu, atau volume.
Penjelasan tersebut dengan memperhatikan komposisi molekuler mereka dan gerakannya.
Dalam buku Kinetic Theory of Gases (2013) karya Walter Kauzman, teori kinetik gas mengatakan bahwa tekanan tidak disebabkan oleh denyut statis di antara molekul.
Tekanan tersebut disebabkan oleh tumbukan antarmolekul yang bergerak pada kecepatan yang berbeda.
Teori kinetik gas memberikan jembatan antara tinjuan gas secara miskroskopik dan makroskopik.
Kata kinetik berasal dari anggapan bahwa molekul gas selalu bergerak. Tiap partikel bergerak bebas dan terjadi tumbukan.
Baca juga: Pengertian Gaya, Rumus, dan Macamnya
Tumbukan tersebut berupa tumbukan lenting sempurna. Dengan sifat tumbukan, maka tidak ada proses kehilangan energi yang dimiliki partikel gas.
Diperlukan obyek gas yang sesuai untuk menyusun partikel gas. Obyek gas tersebut disebut gas ideal.
Terdapat beberapa sifat gas ideal, yaitu:
- Gas terdiri dari partikel padat kecil yang bergerak dengan kecepatan tetap dan dengan arah sembarang.
- Masing-masing partikel bergerak dalam garis lurus, gerakan partikel dipengaruhi oleh tumbukan antara masing-masing partikel atau antara partikel dan dinding.
- Tumbukan antara masing-masing partikel atau partikel dengan dinding adalah tumbukan lenting sempurna.
- Waktu terjadinya tumbukan antar partikel atau antara partikel dengan dinding, sangat singkat dan bisa diabaikan.
- Ukuran volume partikel sangat kecil dibandingkan ukuran volume ruang tempat partikel tersebut bergerak.
Baca juga: Gerak Benda: Cara, Faktor, dan Kegunaannya
Hukum-hukum tentang gas
Gas memiliki beberapa hukum, di antaranya sebagai berikut:
Hukum Boyle
Volume gas dalam suatu ruang tertutup sangat bergantung pada tekanan dan suhunya.
Bila suhu dijaga konstan, maka tekanan yang diberikan akan memperkecil volume.
Bunyi hukum Boyle sebagai berikut:
"Apabila suhu gas yang ada di dalam ruang tertutup dijaga konstan, maka tekanan gas berbanding terbalik dengan volumenya".
Dapat ditulis dengan rumus: