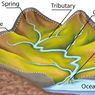
2. Berapa gram massa dari 5,6 liter gas SO2 yang diukur pada 0 derajat celcius, dan tekanan 1 atm jika Ar S= 32 dan Ar O = 16?
Jawaban:
Suhu = 0°C = 0 + 273 = 273 K
Gas SO2 pada suhu 0 derajat celcius atau pada suhu 273 kelvin, berarti gas tersebut berada dalam keadaan STP dengan tekanan 1 atm dan volume satu mol nya 22,4 liter. Tentukan jumlah mol gas SO2 dengan persamaan gas ideal:
PV = nRT
P = tekanan = 1 atm
V = volume gas SO2 = 5,6 liter
n = jumlah mol SO2
R = tetapan gas ideal sebesar 0,082 L atm/mol K
T = suhu = 273 kelvin
PV = nRT
1 x 5,6 = n x 0,082 x 273
n = 5,6 : 22,386 = 0,25 mol
Didapatkan bahwa pada keadaan STP dengan volume 5,6 liter, gas SO2 memiliki jumlah mol sebanyak 0,25 mol. Dari jumlah mol dan massa realtif senyawanya dapat didapatkan massa gas SO2:
Baca juga: Menghitung Reaksi antara Asam Nitrat dan Gas Amonia
 Perhitungan massa gas SO2
Perhitungan massa gas SO2

















































![[POPULER NASIONAL] PDI-P Tahu Arah Pernyataan Wapres | Saudi Deportasi 22 WNI Palsukan Visa Haji](https://asset.kompas.com/crops/k9yMW0DQSWYCnqSKvVORunVlJs0=/0x0:0x0/300x200/data/photo/2024/06/01/665aab9a66d1b.jpeg)