Kesetimbangan Kimia: Menentukan Amonia dalam Jumlah Maksimal

KOMPAS.com - Bahan amonia sangat berguna dalam dunia industri. Contohnya saja, amonia ini digunakan sebagai campuran bahan kimia untuk pupuk urea.
Karena bahan amonia ini sangat penting, suatu usaha untuk memaksimalkan produksi amonia tersebut dapat dilakukan.
Bagaimanakah cara dan usaha-usaha yang dapat dilakukan untuk menghasilkan amonia secara maksimal dengan memanfaatkan ilmu kimia tentang reaksi kesetimbangan kimia? Mari simak pembahasan nya berikut ini.
Soal dan Pembahasan
Pembentukan gas amonia di industri dimulai dengan mencampur gas Nitrogen dengan gas Hidrogen hingga mencapai kesetimbangan yang bersifat eksotermik.
 reaksi pembentukan amonia
reaksi pembentukan amonia
Untuk memperoleh produk gas amonia yang maksimal, reaksi harus bergeser ke arah kanan atau ke arah pembentukan amonia. Hal yang dapat dilakukan agar diperoleh amonia dalam jumlah maksimal adalah…
a. Diberikan inhibitor
b. Volume diperbesar
c. Tekanan diturunkan
d. Suhu dinaikkan setinggi mungkin
e. Konsentrasi gas N2 dan H2 diperbesar
Jawaban: e. Konsentrasi gas N2 dan H2 diperbesar
Baca juga: Menghitung Reaksi antara Asam Nitrat dan Gas Amonia
- Diberikan inhibitor
Dilansir dari ScienceDirect, penambahan inhibitor pada reaksi tidak akan memaksimalkan produk, namun hanya akan menghambat laju reaksi pembentukan amonia.
Pemberian inhibitor menyebabkan amonia akan semakin lambat terbentuk dengan jumlah gas yang dihasilkan tidaklah maksimal.
- Volume diperbesar
Untuk memaksimalkan hasil gas amonia, volume harus diperkecil bukan diperbesar. Memperkecil volume reaktan sama dengan menambah konsentrasi zat sehingga reaksi akan bergeser kearat produk.
- Tekanan diturunkan
Pembentukan amonia reaksinya berada pada fasa zat, sehingga sangat terpengaruh pada perubahan tekanan. Jika tekanan diturunkan, reaksi akan bergeser kearah reaktan sehingga pembentukan amonia tidak maksimal.
Untuk memaksimalkan pembentukan amonia, tekanan harus dinaikkan agar bergeser kearah kanan.
Baca juga: NASA Juno Ungkap Hujan Es Kaya Amonia, Petunjuk Baru Cuaca Planet Jupiter
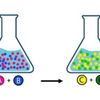
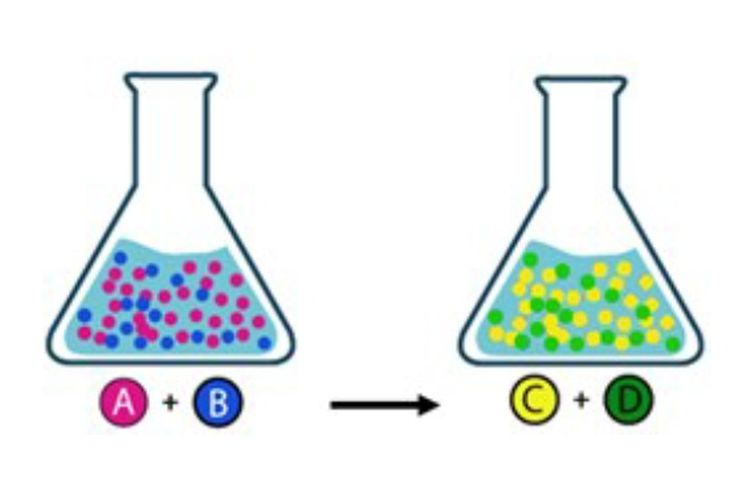 Ilustrasi kesetimbangan kimia.
Ilustrasi kesetimbangan kimia.- Suhu dinaikkan setinggi mungkin
Reaksi diatas merupakan reaksi eksotermik atau reaksi yang melepaskan kalor, berarti panas dapat disebut sebagai produk dari reaksi pembentukan amonia tersebut.
Jika suhu dinaikkan setinggi mungkin, kesetimbangan reaksi akan bergeser kearah kiri dan membentuk lebih banyak reaktan.
Yang harus dilakukan untuk memaksimalkan produk gas amonia adalah menurunkan suhu dari sistem agar kesetimbangannya bergeser kearah kanan.
- Konsentrasi gas N2 dan H2 diperbesar
Ketika konsentrasi reaktan ditambah, pada kasus ini adalah gas N2 dan H2, konsentrasi dan tekanan pada reaktan akan bertambah.
Menurut asas Le Chatelier, saat konsentrasi reaktan bertambah reaksi akan bergeser kearah produk untuk mengurangi ketegangannya, sehingga akan dihasilkan produk yang lebih banyak agar mol keduanya setimbang.
Baca juga: Mewarnai Rambut Tanpa Khawatir dengan Cat Rambut Organik Bebas Amonia
- Bagaimana jika NH3 yang diperbesar konsentrasinya, sedangkan N2 dan H2 tetap?
Jika produk (NH3) konsentrasinya diperbesar, maka reaksi akan bergeser kearah reaktan. Reaksi bergeser kearah kiri untuk mereduksi jumlah mol NH3 dan membentuk gas N2 serta H2 lebih banyak sehingga mencapai kesetimbangan.
Simak breaking news dan berita pilihan kami langsung di ponselmu. Pilih saluran andalanmu akses berita Kompas.com WhatsApp Channel : https://www.whatsapp.com/channel/0029VaFPbedBPzjZrk13HO3D. Pastikan kamu sudah install aplikasi WhatsApp ya.-
![]()
Rumus Tetapan Kesetimbangan
-
![]()
Menghitung Reaksi Kesetimbangan dengan Tetapan Kc
-
![]()
Menghitung Reaksi Kesetimbangan Tetapan Kp
-
![]()
Hubungan Tetapan Kesetimbangan Kc dan Kp
-
![]()
Prinsip Kesetimbangan Kimia dalam Bidang Industri
-
![]()
Menghitung Reaksi antara Asam Nitrat dan Gas Amonia
-
![]()
Soal UAS Kimia: Konsep Kesetimbangan Dinamis