Jadi Penyebab Tak Lulus Uji Fase 1, Apa Pentingnya Kaidah Klinis dalam Pengujian Vaksin Nusantara?

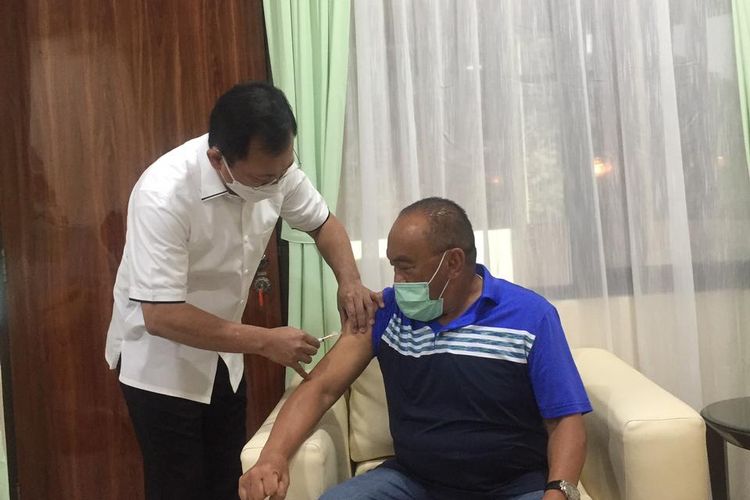
KOMPAS.com - Tersandung masalah kaidah klinis, Vaksin Nusantara inisiasi mantan Menteri Kesehatan Terawan ditangguhkan sementara, karena dinyatakan tidak lulus uji klinik fase 1
Hal ini disampaikan oleh Anggota Tim Advokasi Vaksin Pengurus Besar Ikatan Dokter Indonesia (PB IDI), Dr dr Erlina Burhan MSc SpP(K) dalam diskusi daring bertajuk Menguak Problematika Vaksin Nusantara, Senin (26/4/2021).
"(Vaksin Nusantara) sering mengabaikan evaluasi dari Badan POM dan (pengembangan vaksin) tidak memenuhi kaidah klinis," kata Erlina.
Baca juga: 2 Alasan Ahli Minta Pemerintah dan BPOM Menghentikan Vaksin Nusantara
Tidak hanya itu, Erlina menyebutkan masih banyak pelanggaran yang menyebabkan tidak diizinkannya vaksin Nusantara melanjutkan rencana uji klinis fase II.
Yang mana rencana uji klinis fase II ini kabarnya vaksin Nusantara akan disuntikkan kepada sejumlah tokoh publik dan anggota Komisi IX DPR di RSPAD Gatot Soebroto, Rabu (14/4/2021).
Berikut ini beberapa pelanggaran yang dimaksud:
- Tidak terpenuhi syarat Cara Uji Klinik yang Baik (CUKB)
- Tidak terpenuhi syarat Cara Pembuatan Obat yang Baik (CPOB)
- Tidak terpenuhi syarat Good Laboratory Practice
- Tidak terpenuhi syarat Proof of Concept
- Perbedaan lokasi peneltian (RSUD dr Kariadi Semarang) dengan komite etik (RSPAD Gatot Soebroto)
- Tidak melalui uji praklinik terhadap binatang
- Komponen tidak sesuai pharmaceutical grade (masalah sterilitas) dan kebanyakan diimpor
"Tapi bukan masalah impornya yang tidak disetujui, tetapi memang banyak masalah kaidah klinis penelitian vaksin itu yang harus memenuhi standar," tegas Erlina.
Sebagai informasi, ada dua hal terkait kaidah klinis dalam pengujian vaksin yang perlu Anda ketahui.
1. Standar internasional kaidah klinis dalam pengujian vaksin
Di dunia internasional atau berlaku universal, suatu standar yang disebut The International Conference on Harmonization - Good Clinical Practice (ICH-GCP) digunakan sebagai standar kualitas etik dan ilmiah.
Standar ini dipergunakan untuk dijadikan acuan dalam mendesain, melaksanakan, mencatat, dan melaporkan uji klinik yang melibatkan subyek manusia.
Ditegaskan Erlina, hal ini penting untuk melindungi hak asasi manusia dan juga bentuk upaya menjaga keselamatan manusia yang menjadi subyek uji klinik.
"Jadi standar patient safety (keselataman pasien atau partisipan) itu harus dipertahankan," tegasnya.
Di dalamnya, ICH-GCP mengatur mengenai berbagai hal seperti berikut.
- Prinsip-prinsip dasar
- Dewan Kaji Institusi atau Komite Etik
- Peneliti
- Sponsor
- Protokol dan amandemen protocol
- Brosur peneliti
- Dokumen esensial lainnya
Baca juga: 7 Polemik Vaksin Nusantara, Uji Klinis Lanjut Meski Tak Ada Izin BPOM