Penjelasan Bio Farma, Indonesia Bukan Kelinci Percobaan Vaksin China
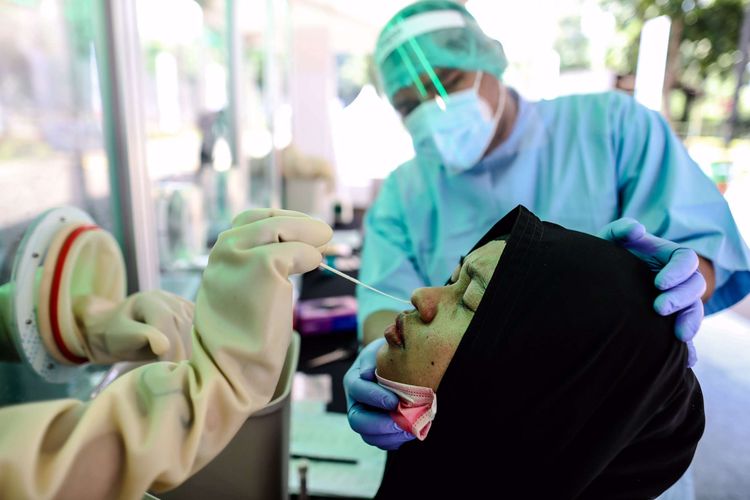
KOMPAS.com - PT Bio Farma menjelaskan secara rinci mengenai tahap uji klinis fase III vaksin virus corona Cinivac dari China yang akan dilakukan pada Agustus 2020.
Sekretaris Perusahaan PT Bio Farma Bambang Heriyanto sekaligus menepis anggapan bahwa uji klinis vaksin Covid-19 ini menjadikan Indonesia sebagai kelinci percobaan vaksin dari China itu.
Anggapan ini muncul setelah ramai dibicarakan di media sosial dan pernyataan sejumlah politisi.
Ia menekankan, uji klinis tahap III ini lebih aman, dan Indonesia justru diuntungkan dari uji ini.
"Kalau menurut kami, kita (Indonesia) beruntung. Karena kita mau melihat respon yang muncul terhadap perbedaan ras, perbedaan geografis, antar negara-negara yang sedang diuji ini," kata Bambang, saat dihubungi Kompas.com, Senin (27/7/2020).
Dengan adanya uji klinis di Indonesia, kata Bambang, maka bisa diketahui kesesuaian vaksin dari Sinovac dengan penduduk Indonesia.
Sementara, jika langsung impor vaksin yang sudah jadi, belum tentu vaksin yang tidak melewati uji klinis di Indonesia akan cocok digunakan.
"Kalau kita dengan uji klinis, nanti kan ketahuan khasiatnya," kata Bambang.
Baca juga: Pemerintah Diminta Jamin Keamanan Relawan Uji Klinis Vaksin Covid-19
Indonesia bukan kelinci percobaan
 Petugas kebersihan menyemprotkan cairan disinfektan di area Pasar Asem Reges, Jakarta Barat, Selasa (21/7/2020). Pengelola Pasar Asem Reges menutup sementara pasar tersebut dari Senin (20/7) hingga Rabu (22/7) menyusul satu orang pedagang terkonfirmasi positif COVID-19 berdasarkan hasil tes usap (swab test).
Petugas kebersihan menyemprotkan cairan disinfektan di area Pasar Asem Reges, Jakarta Barat, Selasa (21/7/2020). Pengelola Pasar Asem Reges menutup sementara pasar tersebut dari Senin (20/7) hingga Rabu (22/7) menyusul satu orang pedagang terkonfirmasi positif COVID-19 berdasarkan hasil tes usap (swab test).Uji klinis di negara lain adalah hal yang biasa. Ia mencontohkan, Bio Farma yang pernah melakukan uji klinis vaksin polio di Belgia dan Panama.
"Fase I-nya di Belgia. Fase II nya di Panama. Apa orang Belgia dan Panama berkata 'Wah ini saya jadi kelinci percobaan ini'. Enggak, ini normal," kata Bambang.
Produk lain dari Bio Farma, yaitu vaksin Pentabio, proses uji klinisnya mulai dari fase I hingga fase III dilakukan di Indonesia. Namun, hal itu tidak pernah diributkan oleh masyarakat.
"Memang seperti itu prosedurnya. Mungkin sekarang ini karena banyak disorot ya jadi kesannya seperti kita jadi kelinci percobaan," kata Bambang.
Selain itu, fase III juga relatif lebih aman dibanding fase I dan II yang sudah dilakukan terlebih dulu di China.
Bambang mengatakan, yang dilakukan Indonesia saat ini adalah mengonfirmasi ulang efek dan khasiat vaksin Sinovac.
Tidak menutup kemungkinan bahwa uji klinis fase III ini akan menemui kegagalan.
Jika demikian, maka pengujian akan dihentikan, penelitian dimulai kembali dari awal, dan izin edar tidak akan dikeluarkan.
Baca juga: [HOAKS] Swab Test Bisa Merusak Otak
Memasuki tahap perizinan
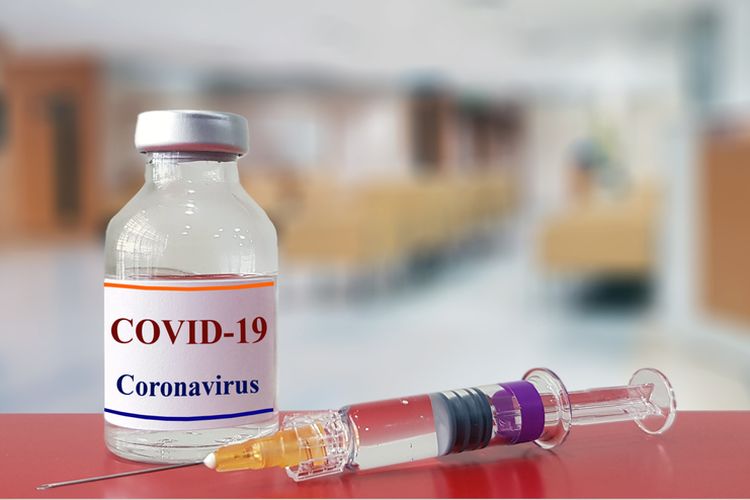
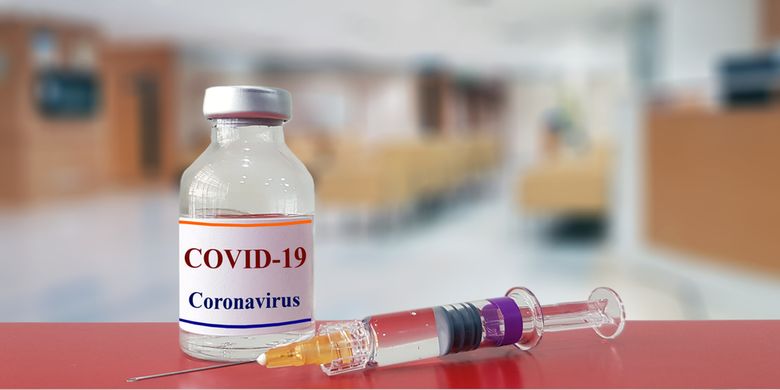 Ilustrasi vaksin corona
Ilustrasi vaksin coronaSebanyak 2.400 vaksin telah diterima oleh Bio Farma dan uji klinis fase III nantinya akan melibatkan lebih dari 1.600 relawan yang akan menjalani pengujian.
Perizinan dibutuhkan untuk melaksanakan uji klinis fase III yang dijadwalkan pada Agustus 2020 dan ditargetkan selesai pada Januari 2021.
Uji klinis ini akan dilakukan oleh lembaga independen, dalam hal ini Fakultas Kedokteran Universitas Padjajaran (FK Unpad).
"Untuk melakukan uji klinis ini ada beberapa izin yang harus ditempuh. Pertama dari Komite Etik yang akan mengawasi uji klinis ini mulai dari awal sampai akhir. Kedua, setelah dari Komite Etik, nanti diproses lebih lanjut di Badan POM untuk mendapatkan Persetujuan Pelaksanaan Uji Klinis (PPUK)," kata Bambang.
Ia mengatakan, PPUK wajib diperoleh karena saat ini vaksin masih dalam tahap riset dan belum memiliki izin edar. Uji klinis fase III ini adalah tahap akhir dalam proses pengembangan vaksin.
"Fase III ini memang paling menentukan. Kalau memang berhasil, maka vaksin bisa digunakan. Kalau tidak berhasil ya kembali nol, harus riset lagi dari awal, cari lagi kandidatnya," kata dia.
Bambang berharap, proses perizinan untuk uji klinis fase III ini bisa selesai pada pekan ini.
Baca juga: Ini Rencana Cadangan jika Tidak Ada Vaksin Corona Tahun Depan
Diuji oleh lembaga independen
 Ilustrasi vaksin virus corona, vaksin Covid-19
Ilustrasi vaksin virus corona, vaksin Covid-19"Bio Farma hanya menyiapkan vaksinnya. Nanti lembaga independen yang menguji. Kalau Bio Farma yang menguji nanti bahaya dong, bisa dikira kongkalikong hasilnya," ujar Bambang.
Sementara, untuk Komite Etik, Bambang mengatakan, dalam tim uji klinis akan ada board executive yang terdiri dari pakar di berbagai bidang, seperti kedokteran dan farmasi, untuk memantau pelaksanaan uji klinis ini.
"Kalau ada nanti terjadi sesuatu, efek samping yang tidak memenuhi syarat, mereka (Komite Etik) yang akan meng-cut 'Oh ini enggak berhasil, nggak boleh dilanjutkan, stop' begitu," kata Bambang.
Selain itu, ada juga pemantauan KIPI (Kejadian Ikutan Pasca Imunisasi). Pemantauan ini melihat dan melakukan review terhadap hasil dari uji klinis, seperti khasiat dari vaksin.
"Karena fase III ini kan untuk melihat khasiat dan efektivitas dari vaksin tersebut di populasi yang besar, termasuk efek sampingnya," kata Bambang.
Vksin yang diterima dari Sinovac sudah dikarantina dan diuji di laboratorium untuk memastikan identitas dan kesterilan, serta kondisi vaksin setelah melewati perjalanan jauh.
"Vaksinnya kita cek dulu di sini, kalau perizinan yang dilakukan tim uji klinis FK Unpad sudah selesai, baru kita kirim. Nanti mereka yang akan menentukan syarat-syarat juga melakukan proses rekrutmen relawan," kata Bambang.
Baca juga: WHO Tegaskan Vaksin Covid-19 Tak Akan Tersedia Tahun Ini, Apa yang Bisa Dilakukan?
Sudah melalui beberapa tahap
 Ilustrasi vaksin corona
Ilustrasi vaksin coronaBaik vaksin ataupun obat sesuai standar WHO harus dilakukan uji dari uji hewan terlebih dahulu atau yang disebut dengan praklinis. Selanjutnya, baru dilakukan uji klinis pada manusia.
Setelah uji praklinis, dilakukan uji pada manusia yang meliputi fase I, II, dan III. Adapun, vaksin Sinovac yang akan diuji klinis di Indonesia telah memasuki fase ketiga.
Uji klinis fase I adalah uji yang digunakan untuk melihat keamanan yang melibatkan sekitar 50-100 orang. Jika fase I ini lulus, baru lanjut ke uji berikutnya.
Adapun uji klinis fase II melibatkan lebih banyak orang yakni sekitar 100-400 orang.
Sementara, fase III untuk melihat khasiat, efektivitas, dan reaksi atau efek samping yang muncul.
Adapun partisipan yang diuji lebih banyak yakni 500-1.000 atau 2.000 orang.
Ia menyebutkan, jika fase ketiga lulus, maka selanjutnya akan lanjut ke tahap perizinan regulator masing-masing negara.
Di Indonesia, melalui BPOM untuk mendapat izin edar di masyarakat. Saat beredar di masyarakat, penggunaannya juga tetap dimonitor.
Baca juga: Uji Klinis Vaksin Corona dari China di Indonesia, Melihat Kerja Sama Bio Farma dan Sinovac
 Infografik: Pencegahan Penularan Virus Corona
Infografik: Pencegahan Penularan Virus Corona
- vaksin
- vaksin corona
- Biofarma
- vaksin Covid-19
- uji klinis vaksin corona
- vaksin corona buatan China
- Sinovac
- vaksin corona dari China
- vaksin covid-19 dari china
- vaksin covid-19 sinovac
- uji klinis vaksin covid-19
- uji klinis vaksin corona
- relawan uji klinis vaksin Covid-19
- relawan uji klinis vaksin virus corona
- relawan uji klinis covid-19 tidak dibayar
-
![]()
AS Lipat Gandakan Anggaran untuk Vaksin Covid-19 Produksi Moderna
-
![]()
Benarkah Indonesia Jadi Kelinci Percobaan Vaksin China? Ini Tanggapan Bio Farma
-
![]()
Ini Rencana Cadangan jika Tidak Ada Vaksin Corona Tahun Depan
-
![]()
WHO Tegaskan Vaksin Covid-19 Tak Akan Tersedia Tahun Ini, Apa yang Bisa Dilakukan?
-
![]()
Uji Klinis Vaksin Corona dari China di Indonesia, Melihat Kerja Sama Bio Farma dan Sinovac
-
![]()
Kenapa Vaksin Virus Corona dari China Diuji di Indonesia? Ini Penjelasan Bio Farma
-
![]()
[POPULER TREN] Vaksin Virus Corona Dijanjikan Siap pada September | Tudingan RS Rekayasa Kasus Covid-19






































![[POPULER TREN] Pabrik Sepatu Bata Purwakarta Tutup | Cara Nonton Indonesia Vs Guinea](https://asset.kompas.com/crops/gwDaIMCZh6kgXAvM2c6Ae0UoCls=/190x359:904x835/177x117/data/photo/2024/05/06/6637c8d7b435b.png)