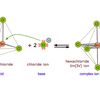
Asam Basa Konjugasi Bronsted Lowry
KOMPAS.com – Salah satu teori yang menyokong ilmu tentang asam dan basa adalah Teori Bronsted Lowry. Dalam Teori Bronsted Lowry ada yang disebut sebagai pasangan asam basa konjugasi.
Apa itu pasangan asam basa konjugasi Bronsted Lowry? Berikut adalah penjelasannya!
Dilansir dari Purdue University College of Science, ciri penting Teori Bronsted Lowry adalah hubungan yang tercipta antara asam dan basa.
Di mana setiap asam Bronsted memiliki basa konjugasi.
Adapun, setiap basa Bronsted memiliki asam konjugasi. Hubungan tersebut disebut sebagai pasangan asam basa konjugasi Bronsted Lowry.
Baca juga: NH4OH: Basa Arrhenius dan Bronsted-Lowry
Pengertian basa konjugasi
Menurut Bronsted Lowry asam adalah spesies apa pun yang menyumbangkan proton (H+).
Dilansir dari Chemistry LibreTexts, asam yang kehilangan proton berubah menjadi basa konjugasinya.
Misalnya, senyawa asam Bronsted HF yang direaksikan dengan air dengan reaksi berikut:
HF(aq) + H2O(l) → F-(aq) + H2O+(aq).
Dalam reaksi tersebut, proton dari HF diikat oleh air (H2O). Sehingga, asam HF yang kehilangan protonnya berubah menjadi basa konjugasi F-.
Baca juga: Teori Asam Basa: Pengertian Para Ahli dan Sifatnya
Pengertian asam konjugasi
Dilansir dari Khan Academy, menurut Bronsted Lowry basa adalah spesies yang dapat menerima proton dan memerlukan pasangan elektron bebas untuk berikatan dengan proton (H+).
Adapun, asam konjugas adalah basa yang telah menerima atau mengikat proton.
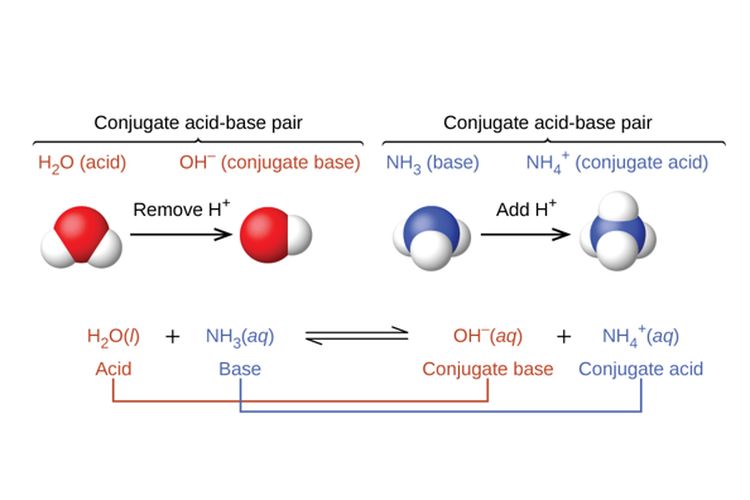
Contohnya adalah senyawa basa NH3 yang bereaksi dengan air sebagai berikut:
NH3(aq) + H2O(l) → NH4+(aq) + OH-(aq).
Dalam reaksi tersebut terlihat bahwa NH3 menerima satu proton dari air. Sehingga, basa NH3 berubah menjadi asam konjugasi NH4-.
Simak breaking news dan berita pilihan kami langsung di ponselmu. Pilih saluran andalanmu akses berita Kompas.com WhatsApp Channel : https://www.whatsapp.com/channel/0029VaFPbedBPzjZrk13HO3D. Pastikan kamu sudah install aplikasi WhatsApp ya.