Perubahan Entalpi pada Reaksi Kimia

KOMPAS.com - Dalam termokimia, perubahan entalpi merupakan salah satu konsep dasar yang sangat penting untuk dipahami. Dilansir dari Chemguide, perubahan entalpi adalah perubahan energi dari awal hingga akhir suatu reaksi kimia.
Perubahan entalpi berkaitan erat dengan hukum kekekalan energi bahwa energi tidak dapat diciptakan ataupun dimusnahkan tapi dapat berubah bentuk menjadi energi lain.
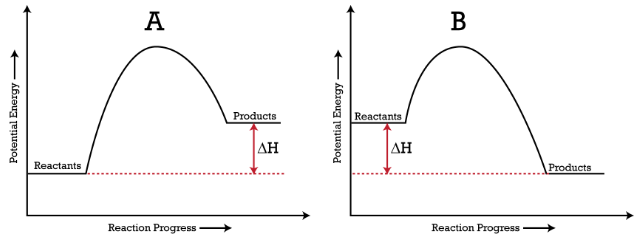 kurva perubahan entalpi
kurva perubahan entalpi
Dari gambar diatas, terlihat bahwa perubahan entalpi adalah selisih dari energi akhir dan energi awal reaksi atau dapat disimpulkan dalam persamaan:
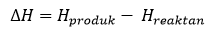 entalpi
entalpi
ΔH = perubahan entalpi reaksi,
ΔH produk = entalpi hasil reaksi,
ΔH reaktan = entalpi awal reaksi.
Baca juga: Energi: Pengertian, Jenis, Satuan, Hukum Kekekalan Energi
Dilansir Khan Academy, jika perubahan entalpi lebih besar dari nol atau bertanda positif maka reaksi tersebut melakukan penyerapan kalor dari lingkungan ke sistem.
Adapun jika nilai entalpi menunjukkan nilai dibawah nol atau negatif, menandakan bahwa sistem tersebut melepaskan energi ke lingkungan sekitarnya.
Untuk memahaminya lebih lanjut, diberikan contoh soal perubahan entalpi sebagai berikut :
 Ilustrasi peristiwa eksotermik yang melibatkan pembakaran
Ilustrasi peristiwa eksotermik yang melibatkan pembakaranContoh soal perubahan entalpi
Jika ΔH CH4 adalah -75 kJ/mol, ΔH2O adalah -242 kJ/mol, ΔH adalah -394 kJ/mol, berapakah perubahan entalpi nya apabila CH4 melalui proses pembakaran dalam kondisi standar?
Baca juga: Hubungan Energi dan Entalpi
- Pembahasan :
Reaksi pembakaran CH4 :
 Reaksi pembakaran dan pembahasan soal perubahan entalpi
Reaksi pembakaran dan pembahasan soal perubahan entalpi
Melansir Chemistry Libretexts, Perubahan entalpi berkaitan erat dengan energi dalam karena entalpi adalah perubahan energi. Entalpi merupakan energi dalam dan usaha yang dilakukan oleh sistem sehingga entalpi dapat disimpulkan dalam persamaan berikut :
 Persamaan entalpi kalor
Persamaan entalpi kalor
H = Entalpi
Q = Kalor
P = tekanan
Energi dalam merupakan total energi yang dimiliki suatu benda dari ikatan molekulernya. Perubahan energi dalam dinyatakan dengan persamaan berikut :
Baca juga: Konsep Energi dan Kemampuan Melakukan Usaha
 rumus energi dal kalor
rumus energi dal kalor
Maka hubungan perubahan entalpi dan energi dalam sebagai berikut :
 Hubungan energi dalam dengan perubahan entalpi
Hubungan energi dalam dengan perubahan entalpi
Dengan H adalah perubahan entalpi, E adalah energi dalam, P adalah tekanan, V adalah perubahan volume. Simak breaking news dan berita pilihan kami langsung di ponselmu. Pilih saluran andalanmu akses berita Kompas.com WhatsApp Channel : https://www.whatsapp.com/channel/0029VaFPbedBPzjZrk13HO3D. Pastikan kamu sudah install aplikasi WhatsApp ya.