Rumus Mencari Mol suatu Unsur

KOMPAS.com – Mol adalah satuan internasional yang mengukur jumlah zat dalam atom, molekul, partikel, ataupun zat kimia lainnya. Bagaimana acara menghitung mol? Untukmengetahuinya, berikut adalah rumus mencari mol!
Rumus mol berdasarkan jumlah partikel
Rumus mol yang pertama adalah yang dikemukakan oleh Amedeo Avogadro dalam hukum Avogradro.
Dilansir dari Encyclopedia Britannica, menurut Avogadro jumlah partikel dalam satu mol adalah sama untuk semua zat. Artinya, jumlah partikel dalam zatu mol zat akan sama dengan jumlah partikel dalam samu mol zat lainnya.
Baca juga: Konsep Mol dan Tetapan Avogadro
Sehingga, rumus molnya menjadi:

JP adalah jumlah partikel. Adapun, 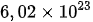 merupakan konstanta Avogadro yang merupakan jumlah partikel dalam satu mol zat.
merupakan konstanta Avogadro yang merupakan jumlah partikel dalam satu mol zat.
Rumus mol berdasarkan massa
Mol juga dapat dihitung dari massa dan massa relatif (Mr) suatu zat. Dilansir dari Lumen Learning, massa satu 1 mol suatu unsur berbeda dengan massa 1 mol unsur lainnya karena massa masing-masing unsur yang berbeda.
Baca juga: Massa Atom Relatif dan Massa Molekul Relatif
Rumus mol berdasarkan massa adalah:

Rumus mol berdasarkan volume gas standar
Mol dapat dihitung melalui volume gas standar yang berada dalam tekanan 1 atm dan suhu 0°C.

Dilansir dari Chemistry LibreTexts, dalam keadaan standar 1 mol gas akan menghabiskan 22,4 L volume wadah.
Baca juga: Sifat-sifat Gas Ideal
Rumus mol berdasarkan volume gas tidak standar
Adapun, mol suatu zat dapat diketahui berdasarkan volume gas yang tidak berada dalam keadaan standar yang diambil dari persamaan gas ideal. Rumus mol berdasarkan volume gas tidak standar adalah:
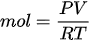
Dengan,
P: tekanan gas (N/m² atau Pa)
V: volume gas (m³)
R: konstanta gas (8,31 J/mol.K)
T: suhu mutlak (K)