Baca berita tanpa iklan. Gabung Kompas.com+
Tekanan Osmotik: Pengertian dan Contoh Soalnya
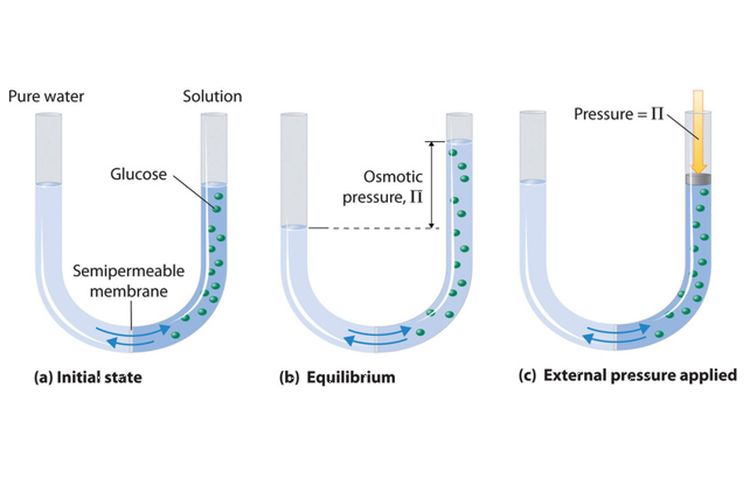
Ilustrasi bagaimana tekanan osmotik menghentikan osmosis pada larutan hipertonis dan hipotonik
Cari soal sekolah lainnya
M=(gram/Mr) × (1.000/V)
=(3,6/180) × (1.000/500)
=0,02 × 2
=0,04 mol/L
Setelah mengetahui molaritasnya, kita dapat menghitung tekanan osmotiknya sebagai berikut:
= M x R x T = 0,04 X 0,082 x 300 = 0,984
Sehingga, tekanan osmosis larutan 3,6 gram glukosa yang terlarut dalam 500 mL adalah sebesar 0,984 atm.
Baca juga: Soal UAS Kimia: Memahami Diagram PT Sifat Koligatif
Contoh soal 2
Berapa tekanan osmotik larutan yang mengandung 46,0 gram gliserin (C3H8O3) per liter pada suhu 0°C?
Jawaban:
Untuk dapat menjawab pertanyaan tersebut, kita harus melalui beberapa tahapan sebagai berikut:
- Merubah satuan suhu dari celcius ke kelvin
T = 0 °C
= 0 °C + 273
= 273 K
- Menentukan massa molekul relatif (Mr) zat terlarut
Mr C3H8O3 = ( 3 x Ar C) + (8 x Ar H) + (3 x Ar O)
= (3 x 12) + (8 x 1) + (3 x 16)
Halaman Berikutnya
= 36 + 8 +…
Video rekomendasi
Video lainnya
Cari soal sekolah lainnya
Rekomendasi untuk anda


































































