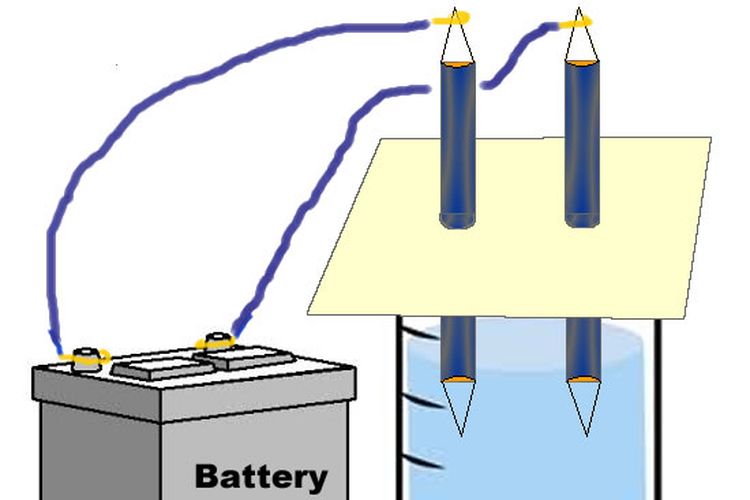
2. Larutan CuSO4 dielektrolisis dengan elektroda inert sehingga menghasilkan 224 mL gas di anoda. Tentukanlah massa endapan yang berada di katoda jika Ar Cu adalah sebesar 63,5!
Jawaban:
Larutan CuSO4 atau tembaga (II) sulfat adalah larutan elektrolit yang dapat terpecah menjadi ion Cu2+ yang bermuatan positif, dan ion SO2- yang bermuatan negatif.
Pada katoda akan menempel muatan positif tembaga (II) sulfat yaitu ion Cu2+ yang kemudian direduksi menjadi endapan tembaga pada katoda dengan reaksi sebagai berikut:
 Reaksi pada katoda
Reaksi pada katoda
Sedangkan pada anodanya hanya akan terjadi oksidasi air menjadi gas oksigen sebanyak 224 mL dengan reaksi berikut:
 Reaksi pada anoda
Reaksi pada anoda
Tentukan jumlah mol unsur Cu dan unsur O hasil reaksi sel elektrolisis, jumlah mol oksigen yang dilepaskan dihitung sesuai dengan perumusan gas pada kondisi STP.
Baca juga: Soal UAS Kimia: Sel Volta
 Perhitungan jumlah mol oksigen
Perhitungan jumlah mol oksigen
Karena ada 4 elektron yang terbentuk saat oksidasi air menjadi gas oksigen, maka jumlah mol pada anodanya harus dikalikan jumlah elektron yang dilepaskan. Jumlah mol anoda adalah 0,01 x 4 = 0,04 mol.
Jumlah mol di anoda harus sama dengan jumlah mol di katoda untuk dapat setimbang, sehingga didapatkan persamaan berikut:
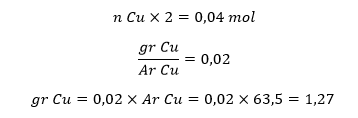 Perhitungan massa endapan katoda
Perhitungan massa endapan katoda
Maka, jumlah endapan logam Cu yang terbentuk di katoda adalah seberat 1,27 gram. Simak breaking news dan berita pilihan kami langsung di ponselmu. Pilih saluran andalanmu akses berita Kompas.com WhatsApp Channel : https://www.whatsapp.com/channel/0029VaFPbedBPzjZrk13HO3D. Pastikan kamu sudah install aplikasi WhatsApp ya.