Perbedaan Larutan Elektrolit dan Larutan Non-Elektrolit
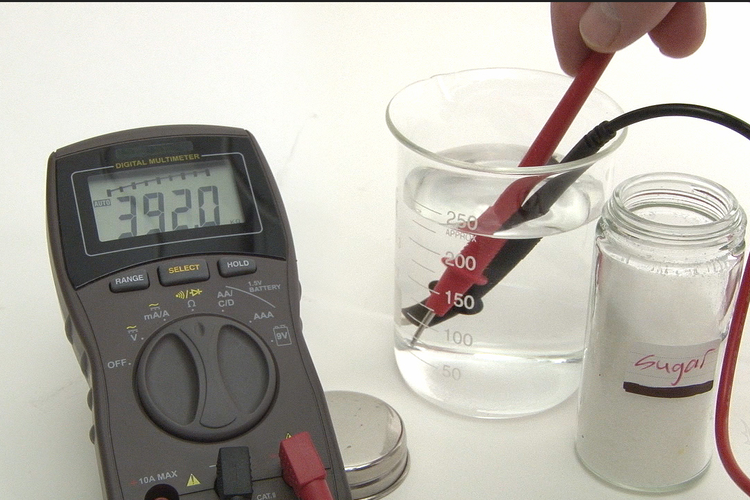
KOMPAS.com - Kamu pasti pernah meminum larutan elektrolit yang baik bagi kesehatan tubuh. Namun apakah sebenarnya larutan elektrolit itu dan apa perbedannya dengan larutan non-elektrolit? Simak penjelasan berikut ini.
Larutan Elektrolit
Larutan elektrolit adalah senyawa kimia yang mengasilkan ion-ion saat dilarutkan kedalam air. Larutan elektrolit dapat menghantarkan listrik selayaknya konduktor karena memiliki ion.
Dilansir dari Encyclopedia Britannica (1998), saat dilarutkan dalam pelarut, senyawa elektrolit mengalami disosiasi menjadi partikel-partikel bermuatan positif dan negative. Partikel-partikel tersebutlah yang disebut sebagai ion.
Sehingga dapat diketahui bahwa senyawa elektrolit terbentuk dari ikatan ion. Contoh larutan elektrolit adalah larutan asam, basa, dan garam.
Baca juga: Larutan Elektrolit dan Ikatan Kimia
Larutan elektrolit dibedakan berdasarkan kekuatannya dalam menghantarkan listrik menjadi larutan elektrolit lemah dan larutan elektrolit kuat. Larutan elektrolit tinggi memiliki derajat ionisasi (α) yang mendekati 1, berarti zat terlarut hampi semuanya terionisasi.
Adapun larutan elektrolit lemah memiliki derajat ionisasi jauh dibawah 1, berarti zat terlarut yang berubah menjadi ion hanya sedikit. Hal ini menyebabkan larutan elektrolit lemah menghantarkan listrik dengan kurang baik.


































































