Model Atom Mekanika Kuantum

KOMPAS.com - Model atom mekanika kuantum adalah model atom paling modern yang digunakan hingga saat ini.
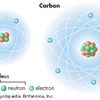
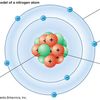
Modelnya berupa atom dengan inti atom dan proton berada ditengah sedangkan elektron mengelilinginya dalam suatu orbital.
Dilansir dari Khan Academy, Erwin Schrodingier adalah ilmuan yang mengemukakan model atom mekanika kuantum berdasakan Prinsip Ketidakpastian Heisenberg dan hipotesis dari Louis de Broglie.
Model atom mekanika kuantum menyatakan bahwa elektron dapat ditemukan berada pada orbital, namun posisinya tidak dapat ditemukan dengan pasti.
Perumpamannya adalah balapan mobil, inti atom dan muatan negatif adalah bagian tengah sirkuit dan juga pit stop yang ada di bagian tengahnya.
Baca juga: Daftar Unsur Kimia Menurut Nomor Atom
Sedangkan orbital adalah jalanan melingkar sirkut tersebut, adapun elektron adalah mobil balap yang berada di sirkuit.
Posisi mobil tidak dapat ditentukan dengan pasti ada di mana. Namun yang pasti mobil tersebut hanya akan berada di jalanan dan bukan di bangku penonton.
Bilangan kuantum pada persamaan gelombang digunakan untuk menentukan kedudukan elektron, bilangan tersebut adalah:
Bilangan Kuantum Utama (n)
Bilangan kuantum utama menyatakan tingkat energi dari atom tersebut. Tingkat energi dapat dikatakan sebagai jumlah orbital atau jalanan elektron yang dimiliki oleh atom tersebut.
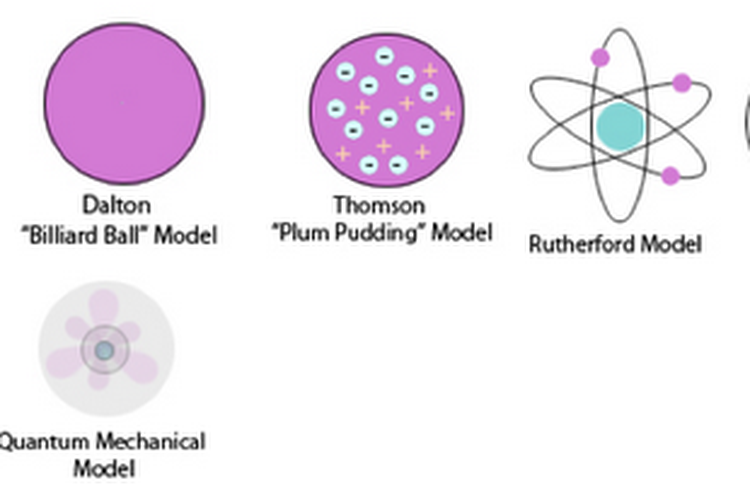 Berbagai model atom sampai model atom mekanika kuantum.
Berbagai model atom sampai model atom mekanika kuantum.Nilai energi diwakilkan oleh banyaknya elektron yang dimiliki atom tersebut. Semakin banyak tingkat energi yang dimiliki oleh suatu atom, maka nilai bilangan kuantum utamanya akan semakin besar.
Bilangan kuantum utama dimulai dari 1,2,3,4,6,8, dan seterusnya.
Bilangan Kuantum Azimuth (l)
Jika bilangan kuantum utama melambangkan kulit atom, maka bilangan kuantum azimuth melambangkan sub kulit atom tempat elektron berada.
Bilangan kuantum azimuth bergantung pada nilai bilangan kuantum utama.
Jika suatu atom memiliki 2 kulit (n=2), maka elektron yanga mungkin berada pada subkulit 2s dan 2p dengan bilangan azimuth (l) yaitu 0 dan 1.
Baca juga: Berkat Muhandis Shiddiq, Komputer Kuantum Lebih Dekat dengan Kenyataan
Bilangan Kuantum Magnetik (m)
Bilangan kuantum magnetik menyatakan orientasi elektron karena berada di dalam medan magnet.
Bilangan kuantum magnetik bergantung pada bilangan kuantum azimuth. Jika bilangan kuantum azimuth bernilai 1, maka bilangan kuatum magnetik bernilai -1, 0, dan +1.
Bilangan Kuantum Spin (s)
Bilangan kuantum spin tidak berhubungan dengan persamaan gelombang, namun menyatakan arah rotasi elektron.
Bilangan kuantum spin hanya ada dua yaitu searah dengan jarum jam (-1/2) dan berlawanan arah dengan jarum jam (+1/2).
Simak breaking news dan berita pilihan kami langsung di ponselmu. Pilih saluran andalanmu akses berita Kompas.com WhatsApp Channel : https://www.whatsapp.com/channel/0029VaFPbedBPzjZrk13HO3D. Pastikan kamu sudah install aplikasi WhatsApp ya.