Pengertian Polarisabilitas dan Contoh Soal

KOMPAS.com - Gaya London adalah salah satu gaya antar molekul yang terjadi karena keberadaan dipol sesaat. Dipol sesaat akan menginduksi atom sekitarnya dan membuat atom tersebut menempel dengan gaya yang disebut gaya London.
Namun tahukah kamu bagaimana dipol sesaat dapat terbentuk dan apa saja yang mempengaruhi pembentukannya? Untuk mengetahuinya, marilah kita simak pembahasan berikut ini!
Dipol sesaat terjadi karena polarisabilitas. Polarisabilitas adalah kemampuan molekul untuk membentuk dipol sesaat ketika diinduksi oleh muatan terdekatnya.
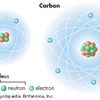
Dilansir dari Chemistry LibreTexts, suatu unsur memiliki susunan elektron yang simetris pada lintasan yang berbentuk bola dan memiliki muatan yang netral.
Namun ketika molekul unsur tersebut dilewatkan arus listrik, elektron dalam atom tersebut akan terdistorsi.
Baca juga: Gaya Antarmolekul: London, van der Waals, dan Ikatan Hidrogen
Elektron akan mengikuti arus listrik membuat salah satu ujung molekul menumpuk elektron (bermuatan negatif) dan ujung lainnya kekurangan elektron (bermuatan positif). Tidak simetrisnya elektron pada atom membuat atom tersebut berubah menjadi dipol sementara.
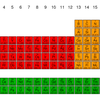
 Perubahan distribusi elektron karena induksi listrik
Perubahan distribusi elektron karena induksi listrik
Satu atom yang berubah menjadi dipol sementara akan merubah atom-atom di sekitarnya menjadi dipol sementara juga. Hal ini mengakibatkan seluruh molekul dapat berubah menjadi dipol dan menyebabkan gaya london.
Maka dapat disimpulkan polarisabilitas adalah kemampuan mudah tidaknya suatu atom terdistorsi oleh muatan lain.
Ada dua faktor yang memengaruhi polarisabilitas suatu atom yaitu jumlah elektron dan orietasi molekul terhadap medan listrik.
Semakin banyak jumlah elektron suatu atom, maka akan semakin banyak jumlah kulit elektron yang dimilikinya.
Baca juga: Konfigurasi Elektron: Prinsip Aufbau, Larangan Pauli, dan Aturan Hund
Hal ini membuat inti atom semakin jauh dengan elektron valensi sehingga semakin sedikit kontrol yang diberikan inti atom. Ini memudahkan atom untuk membentuk dipol sementara.
Kebalikannya, jika jumlah elektronnya sedikit maka semakin sedikit pula jumlah kulitnya. Elektron valensi berada pada posisi yang dekat dengan inti dan sangat terkontrol ini. Hal ini menyebabkan dipol sementara akan lebih sulit dibentuk.
Orientasi molekul terhadap medan listrik dipengaruhi oleh bentuk molekulnya. Dilansir dari Chemguide, molekul dengan bentuk yang asimetris, tipis, dan panjang memiliki polarisabilitas yang tinggi dibanding molekul yang bentuknya simetris.
Hal ini terjadi karena molekulnya asimetris dan elektron dapat bergerak dalam lintasan yang lebih jauh sehingga dipol sesaat lebih mudah terbentuk.
Simak contoh soal polarisabilitas di bawah ini!
Baca juga: Medan Magnet: Menentukan Besar Gaya Lorentz Pada Elektron




















































![[POPULER JABODETABEK] Sopir Fortuner yang Mengaku Adik Jenderal Ditangkap | Pendeta Gilbert Lumoindong Dituduh Nistakan Agama](https://asset.kompas.com/crops/q3uymPBcOVCaM9Sqcb6sffiVe1c=/0x0:0x0/300x200/data/photo/2024/04/17/661f3a6365a6c.jpg)










