Menghitung Reaksi Kesetimbangan Tetapan Kp

Setimbangkan jumlah atom-atom pada reaksi tersebut dengan menambahkan koefisiennya. Atom N dikiri berjumlah 2, maka atom N disebelah kanan juga harus berjumlah 2 dengan menambahkan koefisien 2.
Atom H disebelah kanan berjumlah 6, maka atom H disebelah kiri juga harus berjumlah 6 dengan memberikan koefisien 3 menjadi persamaan berikut:
 Reaksi setimbang pembentukan amonia
Reaksi setimbang pembentukan amonia
Setelah reaksi setimbang, hitunglah mol zat-zat yang bereaksi dan sisa mol zat yang bereaksi. Karena zat nitrogen yang bereaksi hanya setengahnya, maka mol nitrogen yang bereaksi adalah 0,25.
Dari stokiometri persamaan didapatkan perbandingan 1:3:2, berarti gas hidrogen yang bereaksi adalah 3x0,25 mol. Adapun gas ammonia yang terbentuk adalah sebesar 2x0,25 mol.
Baca juga: Rumus Tetapan Kesetimbangan
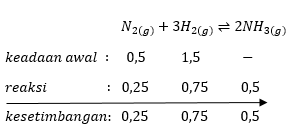 Mol zat-zat yang beraksi
Mol zat-zat yang beraksi
Setelah menentukan konsentrasi zat pada kesetimbangan, tentukan tekanan masing-masing zat pada tekanan 1,5 atm.
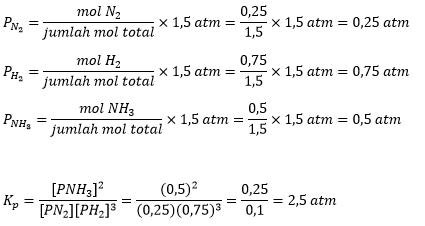 Perhitungan kp reaksi pembentukan amonia
Perhitungan kp reaksi pembentukan amonia
Maka, tetapan kesetimbangan parsial gas reaksi pemebntukan dan penguraian ammonia adalah sebesar 2,5 atm.
Baca juga: Persamaan Reaksi Kimia
Simak breaking news dan berita pilihan kami langsung di ponselmu. Pilih saluran andalanmu akses berita Kompas.com WhatsApp Channel : https://www.whatsapp.com/channel/0029VaFPbedBPzjZrk13HO3D. Pastikan kamu sudah install aplikasi WhatsApp ya.