Logam Alkali: Unsur dan Sifat-sifatnya
KOMPAS.com – Logam alkali adalah salah satu golongan dalam tabel periodik yang sering digunakan dalam kehidupan sehari-hari. Berikut adalah unsur-unsur logam alkali dan sifat-sifatnya!
Unsur-unsur logam alkali
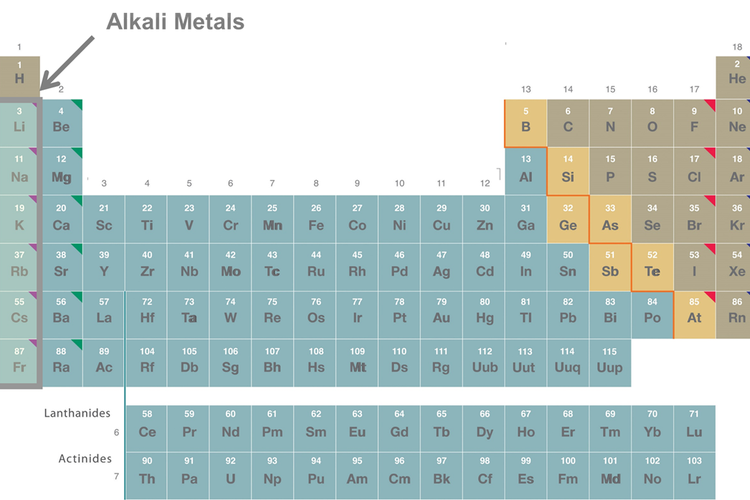
Dalam tabel periodik, logam alkali adalah golongan 1 yang terletak di ujung sebelah kiri dan berada di bawah unsur Hidrogen. Walaupun berada dalam satu kolom, hidrogen bukanlah logam alkali karena merupakan unsur gas.
Logam alkali terdiri dari enam buah unsur yaitu Litium (Li), Natrium (Na), Kalium (K), Rubidium (Rb), Sesium (Cs), dan juga Fransium (Fr). Unsur-unsur tersebut ada yang melimpah di alam, namun ada juga yang tergolong langka.
Unsur natrium dan kaliumlah yang paling melimpah di alam, sedangkan sisanya tergolong langka. Dilansir dari Encyclopedia Britannica, Dalam kerak bumi terdapat 2,6% natrium, 2,4% kalium, 0,03% rubidium, 0,007% litium, dan 0,0007% sesium.
Baca juga: Sifat-Sifat Unsur Kimia
Dengan angka tersebut, rubidium dan sesium sudah tergolong sangat langka. Namun, ternyata fransium jauh lebih langka dan lebih sulit ditemukan di alam.
Sifat-sifat logam alkali
Logam alkali memiliki sifat fisika dan sifat kimia yang unik sehingga mudah dibedakan dengan unsur lainnya. Berikut adalah sifat-sifat unsur dalam golongan logam alkali!
Berkilau
Semua unsur dalam golongan logam alkali memiliki penampakan fisik yang berkilau layaknya perak.
Konduktor yang baik
Seperti logam lainnya, logam alkali merupakan konduktor yang baik. Sebagai konduktor, logam alkali dapat menghantarkan listrik dan juga panas dengan baik.
Baca juga: Gas Mulia: Unsur dan Sifat-sifatnya
Titik didih dan titik leleh yang lebih rendah dari logam lain
Dilansir dari Chemistry Libretexts, ikatan logam dalam logam alkali lebih lemah dari ikatan logam lain sehingga, logam alkali mendidih dan meleleh pada suhu yang lebih rendah daripada logam lain.
Pada golongan alkali, semakin ke bawah maka akan semakin rendah titik didih dan titik leleh unsur tersebut.
Kepadatan yang rendah
Ikatan logam yang lemah juga membuat alkali memiliki kepadatan yang lebih rendah dari logam-logam lainnya. Kepadatan yang rendah membuat logam alkali disebut sebagai logam yang lembut karena bisa dipotong tau dibentuk dengan sangat mudah.
Kepadatan yang rendah berarti massa jenis yang rendah pula. Hal ini membuat beberapa unsur logam alkali (tiga unsur pertama) dapat mengapung di atas air (massa jenisnya lebih rendah dari air).
Baca juga: Ikatan Logam: Definisi, Sifat-Sifat, Pembentukan dan Contohnya
Energi ionisasi yang rendah
Dilansir dari Thought Co, logam alkali memiliki satu elektron di kulit terluar yang terikat secara longgar sehingga jari-jari atomnya besar. Jari-jari atom yang besar mengakibatkan logam alkali memiliki energi ionisasi yang rendah daripada logam lainnya.
Sangat reaktif
Energi ionisasi yang rendah mengakibatkan logam alkali sangatlah reaktif. Artinya, logam alkali sangatlah mudah bereaksi dengan unsur lain.
Logam alkali dapat bereaksi dengan berbagai unsur non logam seperti halogen dan oksigen. Mereka juga bereaksi terhadap udara, bahkan bisa meledak saat bereaksi dengan air.
Mudah membentuk ion positif
Logam alkali memiliki satu elektron valensi, membuatnya mudah membentuk kation (ion positif). Inilah alasan mengapa logam alkali di alam ditemukan dalam bentuk kationnya.
Baca juga: Hantaran Listrik: Konduktor, Isolator, dan Semikonduktor
Reduktif
Dilansir dari Chemistry LibreTexts, kecenderungannya membentuk kation membuat logam alkali sangat tereduksi. Sehingga, dapat menjadi reduktor atau agen pereduksi yang efektif bagi berbagai reaksi kimia.
Simak breaking news dan berita pilihan kami langsung di ponselmu. Pilih saluran andalanmu akses berita Kompas.com WhatsApp Channel : https://www.whatsapp.com/channel/0029VaFPbedBPzjZrk13HO3D. Pastikan kamu sudah install aplikasi WhatsApp ya.
-
![]()
Apa Bedanya Sifat Fisika dan Sifat Kimia?
-
![]()
Sifat Kimia: Pengertian dan Ciri-ciri
-
![]()
Sifat Kimia dan Fisik Air Laut
-
![]()
Sifat-Sifat Unsur Kimia
-
![]()
Ikatan Logam: Definisi, Sifat-Sifat, Pembentukan dan Contohnya
-
![]()
Mengapa Semua Logam Termasuk Konduktor? Jawaban TVRI SD Kelas 4-6
-
![]()
Jenis-Jenis Ikatan Kimia
-
![]()
Gaya Antarmolekul: London, van der Waals, dan Ikatan Hidrogen
-
![]()
Larutan Elektrolit dan Ikatan Kimia